- 身边的化学物质身边的化学物质
- 空气和氧气空气和氧气
- 空气的成分空气的成分
- 氧气的性质和用途氧气的性质和用途
- 氧气的制取氧气的制取
- 水和氢气水和氢气
- 自然界的水自然界的水
- 氢气的性质及制取氢气的性质及制取
- 碳和碳的化合物碳和碳的化合物
- 碳单质碳单质
- 一氧化碳和二氧化碳一氧化碳和二氧化碳
- 二氧化碳的实验室制法二氧化碳的实验室制法
- 金属与金属材料金属与金属材料
- 金属材料金属材料
- 金属的化学性质金属的化学性质
- 金属资源的利用与保护金属资源的利用与保护
- 生活中常见的化合物生活中常见的化合物
- 常见的酸和碱常见的酸和碱
- 中和反应 pH中和反应 pH
- 常见的盐常见的盐
- 复分解反应复分解反应
- 化学肥料化学肥料
- 物质构成和变化物质构成和变化
- 物质的分类物质的分类
- 物质的微粒性物质的微粒性
- 分子分子
- 原子原子
- 离子离子
- 元素元素
- 物质组成的表示物质组成的表示
- 相对原子质量相对原子质量
- 相对分子质量相对分子质量
- 化学式化学式
- 化合价化合价
- 化学方程式化学方程式
- 物质变化物质变化
- 物理变化与化学变化物理变化与化学变化
- 化学反应类型化学反应类型
- 质量守恒定律质量守恒定律
- 金属活动性顺序金属活动性顺序
- 溶液溶液
- 化学基本实验与科学探究化学基本实验与科学探究
- 常用化学仪器常用化学仪器
- 化学实验基本操作化学实验基本操作
- 常见气体的实验室制取常见气体的实验室制取
- 物质鉴别物质鉴别
- 粗盐提纯粗盐提纯
- 粗盐提纯粗盐提纯
- 配制溶质质量分数一定的溶液配制溶质质量分数一定的溶液
- 化学计算化学计算
- 有关化学式的计算有关化学式的计算
- 有关化学方程式的计算有关化学方程式的计算
- 有关溶液的计算有关溶液的计算
- 综合计算综合计算
- 化学与社会发展化学与社会发展
- 人类重要的营养物质人类重要的营养物质
- 化学元素与人类健康化学元素与人类健康
- 有机合成材料有机合成材料
- 化学与能源化学与能源
- 燃烧与灭火燃烧与灭火
- 化石燃料化石燃料
- 能源的利用与开发能源的利用与开发
《一氧化碳和二氧化碳》真题练习
1阅读解答
如图所示是一氧化碳还原氧化铜的实验装置图,回答下列问题:

题目答案
您的答案
答案解析
有下列实验步骤:①加热;②通入一氧化碳。请用上述实验步骤的序号填空,实验开始时,应先,然后。
题目答案
您的答案
答案解析
先通入一氧化碳气体,再加热,目的是排出玻璃管内的空气,避免一氧化碳与空气混合,加热时发生爆炸。
实验进行一段时间后,A装置中出现的现象为。说明有生成,B装置中出现的现象为,说明有生成。
题目答案
您的答案
答案解析
A处黑色的氧化铜在加热条件下被一氧化碳还原为红色的铜,同时产生二氧化碳气体,B处澄清石灰水变浑浊。
装置A中发生反应的化学方程式为____________________,装置B中反应的化学方程式为____________________,装置C的目的是____________________。
题目答案
$CuO + CO \triangleq Cu + CO _ {2}$
$CO _ {2} + Ca ( OH ) _ {2} = CaCO _ {3} \downarrow + H _ {2} O$
除掉一氧化碳,防止环境污染
您的答案
答案解析
一氧化碳能和黑色的氧化铜反应生成红色的铜和二氧化碳,反应的化学方程式为$CuO + CO \triangleq Cu + CO _ {2}$,B处二氧化碳使澄清石灰水变浑浊的化学方程式为$CO _ {2} + Ca ( OH ) _ {2} = CaCO _ {3} \downarrow + H _ {2} O$,一氧化碳有毒,为防止污染大气,可以用燃烧的方法将其处理掉。
反应结束,应先,待冷却后。
题目答案
您的答案
答案解析
实验结束后应先停止加热,冷却后再停止通气体,防止生成的铜在加热的条件下又被氧化为氧化铜。
2单选题
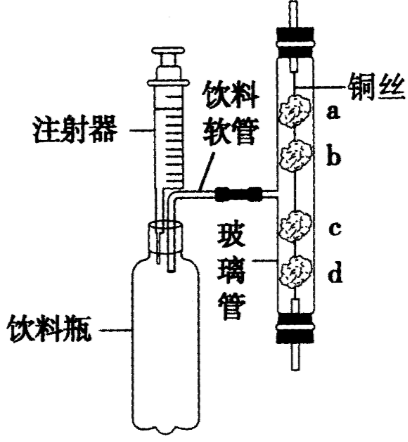
利用生活中的废弃材料来做家庭小实验,其乐无穷!小美同学设计了如图所示的装置(a、d为浸有紫色石蕊试液的湿润棉花,b、c为用紫色石蕊试液浸过的干燥棉花。垂直固定玻璃管的装置未画出)来探究二氧化碳的制取和性质。下列关于该实验装置的叙述不正确的是()
题目答案
您的答案
答案解析
问题要点
酸性溶液能使紫色石蕊变为红色,水、二氧化碳不能单独使紫色石蕊变为红色,从而得出水与二氧化碳反应生成的碳酸能使紫色石蕊变为红色。
通过实验探究来证明二氧化碳确实能与水发生反应生成碳酸。解此类题应注意设计对照实验,进行探究、推理、判断,从而得出正确的结论。
答案解析
通过推压注射器活塞,根据推压的速率可以控制进入饮料瓶内液体的量,选项1-正确;由于稀硫酸与碳酸钙反应生成的硫酸钙微溶于水,利用该装置制取二氧化碳时注射器内的液体不可为稀硫酸,选项2-不正确;利用该装置实验时,由d处的浸有紫色石蕊试液的湿润棉花先变成红色,b、c处浸过紫色石蕊试液的干燥棉花不变色,可验证二氧化碳的密度比空气大及二氧化碳能与水发生反应,选项3-正确;该装置的左半部适用于固液常温下反应制取气体,可以采用该装置利用过氧化氢和二氧化锰反应制取氧气,选项4-正确。
3填空题
二氧化碳是一种温室气体。某化学兴趣小组利用如图6-3-1所示装置对二氧化碳的性质进行验证:

(1)D烧杯中(填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是,具有的化学性质是。
(2)B处紫色石蕊溶液变成红色,C处澄清石灰水变浑浊,B处使紫色石蕊溶液变红的物质是;写出C处发生反应的化学方程式:。
题目答案
您的答案
答案解析
(1)D烧杯内下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明二氧化碳不燃烧也不支持燃烧(化学性质)、密度比空气大(物理性质)。
(2)B处使紫色石蕊溶液变红的物质是碳酸而非二氧化碳;C处澄清石灰水变浑浊,发生反应的化学方程式为$CO _ {2} + Ca ( OH ) _ {2} = CaCO _ {3} \downarrow + H _ {2} O$。
4单选题
一氧化碳有毒是因为它()
题目答案
您的答案
答案解析
选项1-项,可燃性不是毒性,错误;选项2-项,还原性不是毒性,错误;选项3-项,一氧化碳与氧气反应生成二氧化碳,二氧化碳无毒,故错误;选项4-项,一氧化碳极易与血液中的血红蛋白结合,从而使血红蛋白不能再与氧气结合,造成生物体内缺氧,严重时会危及生命,这是一氧化碳有毒的原因,故正确。故选选项4-。
5解答题
(2019秋・崂山区校级月考)利用如图装置验证CO2的性质。回答下列问题:

(1)甲中使石蕊变红的物质是$H _ {2} CO _ {3}$(填化学式)。
(2)乙中反应的文字表达式是氢氧化钙+二氧化碳→碳酸钙+水。
(3)丙中蜡烛由下而上依次熄灭,此现象证明二氧化碳具有密度大于空气的物理性质。
(4)若用装置Ⅰ收集二氧化碳,则气体应从①(填“①”或“②”)端进入;若要检验生成的二氧化碳,可将装置B和装置H用胶皮管连接,并在装置H中盛放澄清的石灰水(填物质名称)试剂。

题目答案
您的答案
答案解析
6单选题
要除去二氧化碳中混有的一氧化碳,可把混合气体通过( )
题目答案
您的答案
答案解析
分析:
根据CO和CO$_2$气体化学性质的差异,选择能与CO发生反应而又不生成气体的物质,在易于操作的条件下,设计合理的方案除去混在二氧化碳中的一氧化气体.
解答:
解:A、一氧化碳不能溶于水,而二氧化碳能溶于水,所以该方案不可行,故A错误;B、混合气体通过炽热的炭层,一氧化碳不与碳反应,二氧化碳气体却与碳反应生成CO而被除去,与题意相违背,所以该方案不可行,故B错误;C、把混合气体通过澄清的石灰水,CO不与氢氧化钙发生反应,而二氧化碳却会因与氢氧化钙发生反应而被除去.方案与意图相违背,该方案不可行,故C错误;D、混合气体通过灼热的氧化铜,气体CO夺取氧化铜的氧而被氧化成二氧化碳,不但可以除去CO气体而且把气体CO转化为二氧化碳;二氧化碳不能与氧化铜发生反应.所以该方案切实可行,故D正确.故选D.
点评:
在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.