- 身边的化学物质身边的化学物质
- 空气和氧气空气和氧气
- 空气的成分空气的成分
- 氧气的性质和用途氧气的性质和用途
- 氧气的制取氧气的制取
- 水和氢气水和氢气
- 自然界的水自然界的水
- 氢气的性质及制取氢气的性质及制取
- 碳和碳的化合物碳和碳的化合物
- 碳单质碳单质
- 一氧化碳和二氧化碳一氧化碳和二氧化碳
- 二氧化碳的实验室制法二氧化碳的实验室制法
- 金属与金属材料金属与金属材料
- 金属材料金属材料
- 金属的化学性质金属的化学性质
- 金属资源的利用与保护金属资源的利用与保护
- 生活中常见的化合物生活中常见的化合物
- 常见的酸和碱常见的酸和碱
- 中和反应 pH中和反应 pH
- 常见的盐常见的盐
- 复分解反应复分解反应
- 化学肥料化学肥料
- 物质构成和变化物质构成和变化
- 物质的分类物质的分类
- 物质的微粒性物质的微粒性
- 分子分子
- 原子原子
- 离子离子
- 元素元素
- 物质组成的表示物质组成的表示
- 相对原子质量相对原子质量
- 相对分子质量相对分子质量
- 化学式化学式
- 化合价化合价
- 化学方程式化学方程式
- 物质变化物质变化
- 物理变化与化学变化物理变化与化学变化
- 化学反应类型化学反应类型
- 质量守恒定律质量守恒定律
- 金属活动性顺序金属活动性顺序
- 溶液溶液
- 化学基本实验与科学探究化学基本实验与科学探究
- 常用化学仪器常用化学仪器
- 化学实验基本操作化学实验基本操作
- 常见气体的实验室制取常见气体的实验室制取
- 物质鉴别物质鉴别
- 粗盐提纯粗盐提纯
- 粗盐提纯粗盐提纯
- 配制溶质质量分数一定的溶液配制溶质质量分数一定的溶液
- 化学计算化学计算
- 有关化学式的计算有关化学式的计算
- 有关化学方程式的计算有关化学方程式的计算
- 有关溶液的计算有关溶液的计算
- 综合计算综合计算
- 化学与社会发展化学与社会发展
- 人类重要的营养物质人类重要的营养物质
- 化学元素与人类健康化学元素与人类健康
- 有机合成材料有机合成材料
- 化学与能源化学与能源
- 燃烧与灭火燃烧与灭火
- 化石燃料化石燃料
- 能源的利用与开发能源的利用与开发
《溶液》真题练习
1单选题
如图所示,四圆分别表示浓溶液、稀溶液、饱和溶液、不饱和溶液的集合,A、B、C、D集合分别表示( )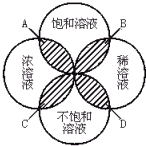
题目答案
您的答案
答案解析
分析:
饱和溶液和不饱和溶液的本质区别是:继续加入该溶质看能否溶解,和溶液的浓稀没有必然的关系.
解答:
解:从图中可以看出A处是饱和溶液和浓溶液的相交的区域,故A是饱和浓溶液;B是饱和溶液和稀溶液的相交处,B是饱和稀溶液;C是不饱和溶液和浓溶液的相交处,C是不饱和浓溶液,D处是不饱和溶液和浓溶液的相交的区域,故D是不饱和浓溶液;故答案:A.饱和浓溶液 B.饱和稀溶液 C.不饱和稀溶液 D.不饱和浓溶液,选A.
点评:
题考查的是有关浓、稀溶液与饱和溶液、不饱和溶液的关系,饱和溶液和不饱和溶液的转化,很好的锻炼了学生对溶液部分基础知识的掌握.
2填空题
图是实验室配制一定溶质质量分数的$NaCl$溶液的流程图。
 (1)应称量g$NaCl$,需加水mL(水的密度为1g/mL)。
(1)应称量g$NaCl$,需加水mL(水的密度为1g/mL)。
(2)某同学按图所示步骤依次操作,其中操作错误的步骤造成配制的溶液的溶质质量分数10%(填“>”“<"”或“=”)。
(3)若称量$NaCl$固体时指针向右偏转,则应直到天平平衡。
(4)取上述正确配制的溶液10g加水稀释到g,可得到5%的$NaCl$溶液。
题目答案
您的答案
答案解析
(1)配制10%的氯化钠溶液50g,需氯化钠的质量为50gx10%=5g;需水的质量为50g-5g=45g,合45mL。
(2)用量筒量取水时,仰视读数,会造成实际量取的水的体积偏大,则溶质质量分数偏小。
(3)称量氯化钠固体时,先放好砝码和调好游码,然后向左边托盘添加氯化钠,若发现指针向右偏转,说明氯化钠的质量小于砝码和游码的质量和,故应继续向左盘添加氯化钠,直至天平平衡。
(4)设稀释后的溶液质量为x,根据溶液稀释前后溶质的质量不变,则$10 g \times 10 \% = x \times 5 \%$,解得x=20g。
3填空题
A、B、C三种固体物质的溶解度曲线如图所示。据图回答问题:

(1)温度为℃时,A与C物质的溶解度相等
(2)将$t _ {1}$℃时A、B、C三种物质的饱和溶液升温到$t _ {2}$℃,有晶体析出的是(填字母代号)。
(3)$t _ {2}$℃时,把A、B物质各50$g$分别加到100$g$水中,不能形成饱和溶液的是(填字母代号),若要使之恰好达到饱和状态,还需要向溶液中加入$g$该溶质。
(4)若A中含有少量B,应用法提纯。
(5)图中物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似
题目答案
您的答案
答案解析
(1)$t _ {1}$℃时,A与C物质的溶解度相等。
(2)C物质的溶解度随温度的升高而减小,将$t _ {1}$℃时C物质的饱和溶液升温到$t _ {2}$℃,会析出固体。
(3)$t _ {2}$℃时,A物质的溶解度是80$g$B物质的溶解度是50$g$,把A、B物质各50$g$分别加到100$g$水中,A物质不能形成饱和溶液,若要使之恰好达到饱和状态,还需要向溶液中加入溶质的质量为80$g$-50$g$=30$g$。
(4)A物质的溶解度受温度的影响较大,B物质的溶解度受温度的影响较小,若A中含有少量B,应用降温结晶的方法提纯。
(5)气体的溶解度随温度的升高而减小,所以C物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似。
4单选题
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是()

题目答案
您的答案
答案解析
由溶解度曲线可知,$t _ {1} ^ {\circ} C$时乙的溶解度大于甲的溶解度,选项1-错误;丙的溶解度随温度的升高而降低,所以降温不能使接近饱和的丙溶液变成饱和溶液,选项2-错误;将$t _ {2} ^ {\circ} C$甲、乙、丙的饱和溶液降温至$t _ {1} ^ {\circ} C$,所得溶液的溶质质量分数:乙>甲>丙,选项3-错误。
5填空题
甲、乙、丙三种物质的溶解度曲线如图所示。请回答下列问题:

(1)在0℃-60℃之间,三种物质中溶解度受温度影响最小的是。
(2)20℃时,三种物质的溶解度由小到大的顺序为。
(3)在不改变溶液中溶质质量分数的前提下,要使接近饱和的丙溶液变为饱和溶液,可采取的一种措施是。
(4)50℃时,将甲、乙、丙各20g分别加入盛有50g水的烧杯中,充分溶解,静置,然后各取上层清液mg,再降温至10℃,此时三种溶液中溶质的质量分数分別为$\omega$(甲)、$\omega$(乙)、$\omega$(丙),则三者之间的大小关系是。
题目答案
您的答案
答案解析
解题思路
(1)根据溶解度曲线可以判断,甲、丙的溶解度受温度影响较大,乙的溶解度受温度影响较小。
(2)20℃时,三种物质的溶解度由小到大的顺序为丙<甲<乙。
(3)丙的溶解度随温度升高而降低,可以通过升温的方法使接近饱和的丙溶液变为饱和溶液。
(4)50℃时,将甲、乙、丙各20g分别加入盛有50g水的烧杯中,充分溶解得到甲、乙的不他和溶液,丙的饱和溶液,取上层清液,再降温到10℃,甲、乙溶液中有晶体析出,且甲溶液析出的晶体比乙多,所以此时三种溶液中溶质的质量分数为$\omega$(乙)>$\omega$(甲)>$\omega$(丙)。
6单选题
小叶同学在做家庭小实验时,把下列物质分别放入足量水中充分搅拌,不能形成溶液的是( )
题目答案
您的答案
答案解析
分析:
一种或几种物质分散到另一种物质中,形成均一的、稳定的混合物叫做溶液,它的基本特征是均一性和稳定性;只有被分散的物质在水中是可溶的,二者混合后才会形成溶液.
解答:
A、白酒易溶于水,形成均一、稳定的混合物,属于溶液;故选项错误.B、味精易溶于水,形成均一、稳定的混合物,属于溶液;故选项错误.C、食盐易溶于水,形成均一、稳定的混合物,属于溶液;故选项错误.D、花生油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液;故选项正确.故选D.
点评:
本题难度不大,掌握溶液的本质特征、各种物质的水溶性方面的知识是解答本题的关键.