- 身边的化学物质身边的化学物质
- 空气和氧气空气和氧气
- 空气的成分空气的成分
- 氧气的性质和用途氧气的性质和用途
- 氧气的制取氧气的制取
- 水和氢气水和氢气
- 自然界的水自然界的水
- 氢气的性质及制取氢气的性质及制取
- 碳和碳的化合物碳和碳的化合物
- 碳单质碳单质
- 一氧化碳和二氧化碳一氧化碳和二氧化碳
- 二氧化碳的实验室制法二氧化碳的实验室制法
- 金属与金属材料金属与金属材料
- 金属材料金属材料
- 金属的化学性质金属的化学性质
- 金属资源的利用与保护金属资源的利用与保护
- 生活中常见的化合物生活中常见的化合物
- 常见的酸和碱常见的酸和碱
- 中和反应 pH中和反应 pH
- 常见的盐常见的盐
- 复分解反应复分解反应
- 化学肥料化学肥料
- 物质构成和变化物质构成和变化
- 物质的分类物质的分类
- 物质的微粒性物质的微粒性
- 分子分子
- 原子原子
- 离子离子
- 元素元素
- 物质组成的表示物质组成的表示
- 相对原子质量相对原子质量
- 相对分子质量相对分子质量
- 化学式化学式
- 化合价化合价
- 化学方程式化学方程式
- 物质变化物质变化
- 物理变化与化学变化物理变化与化学变化
- 化学反应类型化学反应类型
- 质量守恒定律质量守恒定律
- 金属活动性顺序金属活动性顺序
- 溶液溶液
- 化学基本实验与科学探究化学基本实验与科学探究
- 常用化学仪器常用化学仪器
- 化学实验基本操作化学实验基本操作
- 常见气体的实验室制取常见气体的实验室制取
- 物质鉴别物质鉴别
- 粗盐提纯粗盐提纯
- 粗盐提纯粗盐提纯
- 配制溶质质量分数一定的溶液配制溶质质量分数一定的溶液
- 化学计算化学计算
- 有关化学式的计算有关化学式的计算
- 有关化学方程式的计算有关化学方程式的计算
- 有关溶液的计算有关溶液的计算
- 综合计算综合计算
- 化学与社会发展化学与社会发展
- 人类重要的营养物质人类重要的营养物质
- 化学元素与人类健康化学元素与人类健康
- 有机合成材料有机合成材料
- 化学与能源化学与能源
- 燃烧与灭火燃烧与灭火
- 化石燃料化石燃料
- 能源的利用与开发能源的利用与开发
《有关化学方程式的计算》真题练习
1解答题
用石灰石泥浆吸收工业废气中的$SO_{2}$,可以有效减少$SO_{2}$的排放。若用12.5t含$CaCO_{3}$80%的石灰石配成泥浆,理论上$CaCO_{3}$能完全吸收二氧化硫的质量为多少?(该反应的化学方程式为$2CaCO_{3}+O_{2}+2SO_{2}\stackrel{高温}{=}2CaSO_{4}+2CO_{2}$)
题目答案
解:设理论上能完全吸收$SO_{2}$的质量为x。

$\frac {200} {12.5 t \times 80 \%} = \frac {128} {x} \quad x = 6.4 t$
答:理论上可吸收$SO_{2}$的质量为6.4t。
您的答案
答案解析
题中已知数据12.5t是石灰石(混合物)的质量,而化学方程式中参与反应的是石灰石中的$CaCO_{3}$,计算时应先将石灰石质量换算成$CaCO_{3}$质量,再根据化学方程式计算。
2解答题
6.2g磷在空气中完全燃烧,生成五氧化二磷多少克?消耗空气多少升?(标准状况下氧气的密度为1.43g/L)
题目答案
解:设生成五氧化二磷的质量为x,参加反应的氧气的质量为y。

$\frac {124} {284} = \frac {6.2 g} {x} \quad x = 14.2 g$
$\frac {124} {160} = \frac {6.2 g} {y} \quad y = 8 g$
氧气的体积为$\frac {8 g} {1.43 g / L} \approx 5.59 L$
消耗空气的体积约为$5.59L×5=27.95L$
答:生成五氧化二磷14.2g,消耗空气27.95L。
您的答案
答案解析
问题要点
方法技巧:
根据化学方程式计算的一般解题思路:(1)先找出题中涉及的化学反应,并正确写出化学方程式;(2)分析题中已知数据与方程式中各物质的直接或间接关系;(3)确定哪些数据能直接代入方程式,若所给数据不能代入方程式,则要分析清楚该数据如何转化成方程式中物质的数据,再列出相应比例式。
答案解析
涉及体积、密度的计算要注意体积、质量、密度的关系,同时要注意体积、密度、质量之间的单位是否统一。只有质量数据才能直接代入化学方程式计算。
3解答题
将氯酸钾和二氧化锰的固体混合物20g加入试管中,加热。待完全反应后,将试管冷却、称量,试管内固体物质为15.2g。计算:
(1)反应生成的氧气质量为_____g。
(2)列式计算原固体混合物中氯酸钾的质量。
题目答案
(1)4.8
(2)解:设原固体混合物中氯酸钾的质量为x。

$\frac {245} {96} = \frac {x} {4.8 g}$
$x = 12.25 g$
答:原固体混合物中氯酸钾的质量为12.25g。
您的答案
答案解析
问题要点
该例题取材于实验室用高锰酸钾制氧气,已知反应物高锰酸钾的质量求反应生成氧气的质量,属于根据化学方程式计算的基础题,将6.3g高锰酸钾代入化学方程式即可求解。
根据化学方程式进行的简单计算。在解答时要注意计算格式的规范性,如设未知量、书写化学方程式和相关量、列比例式、求解、作答等,明确利用化学方程式的简单计算的前提是正确书写化学方程式以及找出反应物与生成物的质量关系。
答案解析
根据质量守恒定律可知,反应过程中质量的减少是因为生成了氧气,生成氧气的质量为20g-15.2g=4.8g;根据氧气的质量和相应的化学方程式即可计算出固体混合物中氯酸钾的质量。
4阅读解答
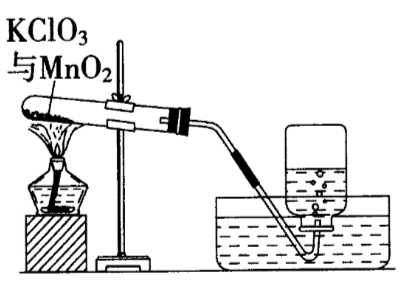
某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g。
加热时间/min | 0 | $t _ {1}$ | $t _ {2}$ | $t _ {3}$ |
固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
题目答案
您的答案
答案解析
共制得氧气g。
题目答案
您的答案
答案解析
加热前固体的总质量为28.0g,反应开始后,因生成氧气,固体质量不断减少,当固体质量不再减少时,说明氯酸钾已全部分解,此时共制得氧气的质量为28.0g-18.4g=9.6g。
计算所得氯化钾溶液中所含氯化钾的质量。
题目答案
解:设反应生成氯化钾的质量为x。

$\frac {149} {96} = \frac {x} {9.6 g} \quad x = 14.9 g$
答:所得氯化钾溶液中所含氯化钾的质量为14.9g。
您的答案
答案解析
问题要点
解答此类题的关键在于依据质量守恒定律,利用反应前后固体质量的差值,求出反应中生成氧气的质量,以此作为突破口,求出其他物质的质量。
答案解析
根据化学方程式,利用生成氧气的质量可求出生成氯化钾的质量。