- 第八单元 金属和金属材料第八单元 金属和金属材料
- 课题1 金属材料课题1 金属材料
- 几种重要的金属几种重要的金属
- 合金合金
- 课题2 金属的化学性质课题2 金属的化学性质
- 金属与氧气的反应金属与氧气的反应
- 金属与盐酸、稀硫酸的反应金属与盐酸、稀硫酸的反应
- 置换反应置换反应
- 金属与其他金属化合物溶液的反应金属与其他金属化合物溶液的反应
- 金属活动性顺序金属活动性顺序
- 课题3 金属资源的利用和保护课题3 金属资源的利用和保护
- 金属资源的存在形式及常见的矿石金属资源的存在形式及常见的矿石
- 铁的冶炼铁的冶炼
- 有关化学反应中杂质问题的计算有关化学反应中杂质问题的计算
- 金属资源保护金属资源保护
- 实验活动4 金属的物理性质和某些化学性质实验活动4 金属的物理性质和某些化学性质
- 第九单元 溶液第九单元 溶液
- 课题1 溶液的形成课题1 溶液的形成
- 溶液溶液
- 溶解时的吸热或放热现象溶解时的吸热或放热现象
- 乳化现象乳化现象
- 课题2 溶解度课题2 溶解度
- 饱和溶液饱和溶液
- 固体溶解度固体溶解度
- 气体溶解度气体溶解度
- 课题3 溶液的浓度课题3 溶液的浓度
- 溶质质量分数溶质质量分数
- 溶液的计算溶液的计算
- 溶液的配制溶液的配制
- 实验活动5 一定溶质质量分数的氯化钠溶液的配制实验活动5 一定溶质质量分数的氯化钠溶液的配制
- 第十单元 酸和碱第十单元 酸和碱
- 课题1 常见的酸和碱课题1 常见的酸和碱
- 酸、碱与指示剂作用酸、碱与指示剂作用
- 常见的酸常见的酸
- 常见的碱常见的碱
- 课题2 酸和碱的中和反应课题2 酸和碱的中和反应
- 中和反应中和反应
- 中和反应在实际中的应用中和反应在实际中的应用
- 溶液酸碱度的表示法——pH溶液酸碱度的表示法——pH
- 了解溶液酸碱性的重要意义了解溶液酸碱性的重要意义
- 实验活动6 酸、碱的化学性质实验活动6 酸、碱的化学性质
- 实验活动7 溶液酸碱性的检验实验活动7 溶液酸碱性的检验
- 第十一单元 盐 化肥第十一单元 盐 化肥
- 课题1 生活中常见的盐课题1 生活中常见的盐
- 氯化钠氯化钠
- 粗盐提纯粗盐提纯
- 碳酸钠、碳酸氢钠和碳酸钙碳酸钠、碳酸氢钠和碳酸钙
- 复分解反应复分解反应
- 盐的化学性质盐的化学性质
- 课题2 化学肥料课题2 化学肥料
- 常见化肥的种类和作用常见化肥的种类和作用
- 使用化肥、农药与环境的关系使用化肥、农药与环境的关系
- 化肥的简易鉴别化肥的简易鉴别
- 实验活动8 粗盐中难溶性杂质的去除实验活动8 粗盐中难溶性杂质的去除
- 第十二单元 化学与生活第十二单元 化学与生活
- 课题1 人类重要的营养物质课题1 人类重要的营养物质
- 课题2 化学元素与人体健康课题2 化学元素与人体健康
- 课题3 有机合成材料课题3 有机合成材料
《金属与盐酸、稀硫酸的反应》题目练习
1单选题
现有等质量甲、乙、丙三种金属,分别放入三份浓度相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中的化合价均为+2)。则下列说法中错误的是()
题目答案
您的答案
答案解析
根据图像的“坡度”可确定金属活动性顺序:乙>甲>丙,选项A正确;根据图像的“高度”可确定三种金属完全反应生成氢气的质量:甲>乙>丙,选项B正确;由于三种金属在生成物中的化合价相同、质量相等,所以产生的氢气质量与金属的相对原子质量成反比,产生氢气质量越多,说明该金属的相对原子质量越,则相对原子质量:丙>乙>甲,选项C错误;由质量守恒定律可知,生成氢气的质量等于参加反应的稀硫酸中氢元素的质量,生成氢气的质量越多,消耗稀硫酸的质量越多,则消耗稀硫酸的质量:甲>乙>丙,选项D正确。
2单选题
金属与盐酸反应的示意图如图所示,下列说法正确的是()

题目答案
您的答案
答案解析
问题要点
解答此类问题应明确:不同金属与酸反应的剧烈程度不同(可根据产生气泡的快慢判断),且有些金属(如铜)不与稀盐酸和稀硫酸反应;铁与稀盐酸或稀硫酸反应生成含亚铁离子的化合物。
答案解析
由于在金属活动性顺序中铜位于氢后,所以铜和稀盐酸不反应,选项A错误;由示意图知,镁产生气泡的速率最快,所以镁与稀盐酸反应速率最快,在四种金属中活动性最强,选项B正确;稀盐酸中不含氢气,选项C错误;铁和稀盐酸反应生成氯化亚铁和氢气,选项D错误。
3阅读解答
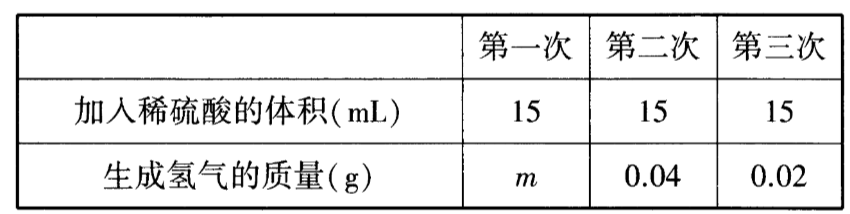
黄铜是铜和锌的合金。某化学兴趣小组的同学欲测定实验室中某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量10$g$粉末状黄铜样品放入烧杯中,量取45$mL$稀硫酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如下表:
题目答案
您的答案
答案解析
m的数值是。
题目答案
您的答案
答案解析
由第二次、第三次实验数据可知,15$mL$稀硫酸完全反应生成氢气质量是0.04$g$,因此m的数值是0.04。
此黄铜样品中铜的质量分数是多少?(写出计算过程)
题目答案
解:设黄铜样品中锌的质量为x
反应生成氢气质量:$0.04 g + 0.04 g + 0.02 g = 0.1g$

样品中铜的质量分数是$\frac {10 g - 3.25 g} {10 g} \times 100 \% = 67.5 \%$
答:此黄铜样品中铜的质量分数是$67.5 \%$。
您的答案
答案解析
合金中的锌完全反应,生成氢气质量为$0.04 g + 0.04 g + 0.02 g =$$0.1 g$,根据锌与稀硫酸反应的化学方程式,由氢气的质量可以计算出锌的质量,从而可以计算黄铜样品中铜的质量分数。
4单选题
下列物质中,能由金属跟盐酸直接反应制取的是()
题目答案
您的答案
答案解析
铁与盐酸反应的产物为氯化亚铁;不是氯化铁,选项A错误;
银不能置换出盐酸中的氢,无法生成$AgCl$,选项B错误;
锌能与盐酸反应生成氯化锌,选项C正确;
铜不能置换出盐酸中的氢,无法生成$CuCl _ {2}$,选项D错误。
5单选题
苹果、梨等多种水果的细胞中都含有輮酸。鞣酸能和铁反应,生成黑色的鞣酸铁与氢气,所以苹果、梨用铁刀切开以后,表面会变黑。下列四种金属中,能与鞣酸反应生成氢气的是()
题目答案
您的答案
答案解析
金属活动性顺序中,排在氢前面的金属,能与酸反应生成氢气,四种金属中只有锌能与酸反应生成氢气。
6单选题
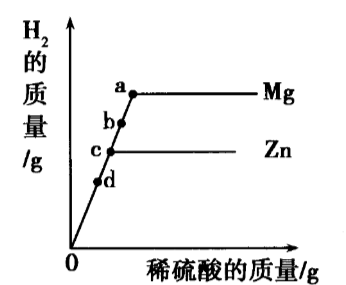
两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加人稀硫酸的质量关系如图所示。下列说法正确的是()
题目答案
您的答案
答案解析
a点时,镁与稀硫酸恰好完全反应,锌早已完全反应:b点时,镁与稀硫酸反应产生的氢气多,锌与稀硫酸反应产生的氢气少;c点时,锌与稀硫酸恰好完全反应,镁有剩余;d点时,锌与镁均还没有完全反应,两个烧杯中都有金属剩余。
7单选题
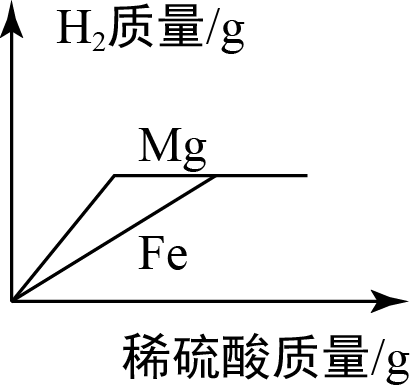
将质量相等的镁粉和铁粉分别投入等质量等浓度的稀硫酸中,所得 ${{\text{H}}_2}$ 质量与稀硫酸质量关系曲线正确的是( )
题目答案
您的答案
答案解析
反应的稀硫酸质量相等时,生成氢气质量也相等,最终镁和稀硫酸反应生成的氢气多,$\rm B$ 对应关系正确;
故选 $\rm B$。