- 第八单元 金属和金属材料第八单元 金属和金属材料
- 课题1 金属材料课题1 金属材料
- 几种重要的金属几种重要的金属
- 合金合金
- 课题2 金属的化学性质课题2 金属的化学性质
- 金属与氧气的反应金属与氧气的反应
- 金属与盐酸、稀硫酸的反应金属与盐酸、稀硫酸的反应
- 置换反应置换反应
- 金属与其他金属化合物溶液的反应金属与其他金属化合物溶液的反应
- 金属活动性顺序金属活动性顺序
- 课题3 金属资源的利用和保护课题3 金属资源的利用和保护
- 金属资源的存在形式及常见的矿石金属资源的存在形式及常见的矿石
- 铁的冶炼铁的冶炼
- 有关化学反应中杂质问题的计算有关化学反应中杂质问题的计算
- 金属资源保护金属资源保护
- 实验活动4 金属的物理性质和某些化学性质实验活动4 金属的物理性质和某些化学性质
- 第九单元 溶液第九单元 溶液
- 课题1 溶液的形成课题1 溶液的形成
- 溶液溶液
- 溶解时的吸热或放热现象溶解时的吸热或放热现象
- 乳化现象乳化现象
- 课题2 溶解度课题2 溶解度
- 饱和溶液饱和溶液
- 固体溶解度固体溶解度
- 气体溶解度气体溶解度
- 课题3 溶液的浓度课题3 溶液的浓度
- 溶质质量分数溶质质量分数
- 溶液的计算溶液的计算
- 溶液的配制溶液的配制
- 实验活动5 一定溶质质量分数的氯化钠溶液的配制实验活动5 一定溶质质量分数的氯化钠溶液的配制
- 第十单元 酸和碱第十单元 酸和碱
- 课题1 常见的酸和碱课题1 常见的酸和碱
- 酸、碱与指示剂作用酸、碱与指示剂作用
- 常见的酸常见的酸
- 常见的碱常见的碱
- 课题2 酸和碱的中和反应课题2 酸和碱的中和反应
- 中和反应中和反应
- 中和反应在实际中的应用中和反应在实际中的应用
- 溶液酸碱度的表示法——pH溶液酸碱度的表示法——pH
- 了解溶液酸碱性的重要意义了解溶液酸碱性的重要意义
- 实验活动6 酸、碱的化学性质实验活动6 酸、碱的化学性质
- 实验活动7 溶液酸碱性的检验实验活动7 溶液酸碱性的检验
- 第十一单元 盐 化肥第十一单元 盐 化肥
- 课题1 生活中常见的盐课题1 生活中常见的盐
- 氯化钠氯化钠
- 粗盐提纯粗盐提纯
- 碳酸钠、碳酸氢钠和碳酸钙碳酸钠、碳酸氢钠和碳酸钙
- 复分解反应复分解反应
- 盐的化学性质盐的化学性质
- 课题2 化学肥料课题2 化学肥料
- 常见化肥的种类和作用常见化肥的种类和作用
- 使用化肥、农药与环境的关系使用化肥、农药与环境的关系
- 化肥的简易鉴别化肥的简易鉴别
- 实验活动8 粗盐中难溶性杂质的去除实验活动8 粗盐中难溶性杂质的去除
- 第十二单元 化学与生活第十二单元 化学与生活
- 课题1 人类重要的营养物质课题1 人类重要的营养物质
- 课题2 化学元素与人体健康课题2 化学元素与人体健康
- 课题3 有机合成材料课题3 有机合成材料
《盐的化学性质》题目练习
1单选题
如图是实验室里一瓶标签破损的白色粉末状固体。小明同学取出少量该固体放入一洁净试管中,加水振该后固体溶解,形成无色透明溶液,继续加人少量盐酸,有无色无味的气体产生,该固体可能是()
![]()
题目答案
您的答案
答案解析
根据破损的标签可知,该物质中含有钠元素,由题中信息“取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续加入少量盐酸,有无色无味的气体产生”可知,该固体可能是碳酸氢钠,碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,选项A正确。
2单选题
某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,进行如下实验:①取少量固体加入足量的水,搅拌,有不溶物;②过滤,向滤液中加入盐酸,有气泡产生。下列对固体粉末成分的判断中,不正确的是()
题目答案
您的答案
答案解析
根据实验①能确定不溶物为碳酸钙,但不能确定此不溶物是原来固体粉末中的碳酸钙,还是$Ca ( OH ) _ {2}$与$Na _ {2} CO _ {3}$反应生成的碳酸钙,选项2-错误;氢氧化钙与碳酸钠反应生成碳酸钙白色沉淀,而与稀盐酸反应无明显现象,故无法确定固体粉未中是否存在氢氧化钙,选项4-正确;根据实验②向滤液中加入盐酸有气泡产生,说明固体粉末中一定含有碳酸钠,选项1-正确;在这两步实验中,氢氧化钠可能不参加反应,即使参加反应也无明显现象,所以固体粉末中有没有氢氧化钠也无法确定,选项3-正确。
3单选题
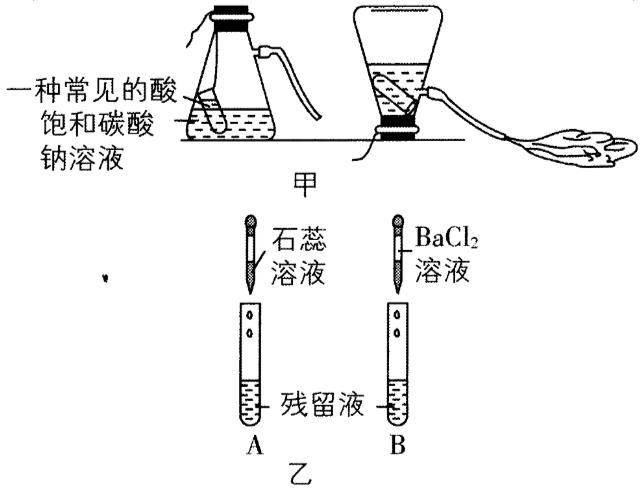
利用饱和碳酸钠溶液与酸反应,小科同学做了如图甲所示的简易酸碱灭火器装置,并进行操作。操作结束后,对瓶中残留液进行如图乙所示的实验,实验现象为A试管溶液变红色,B试管中有白色沉淀生成,则残留液中含有的溶质有()
题目答案
您的答案
答案解析
对瓶中残留液进行如图乙所示的实验,A试管溶液变红色,说明甲中反应的酸过量,B试管中有白色沉淀生成,结合A试管中实验现象可知,反应后溶液中含有硫酸根离子,因此反应物中的酸是硫酸,则残留液中含有的溶质有反应生成的硫酸钠和过量的硫酸,选项C正确。
4单选题
只用一种试剂来鉴别$KOH$、$Ca ( OH ) _ {2}$、稀盐酸三种溶液,这种试剂是( )
题目答案
您的答案
答案解析
选项1-项,氯化铜溶液与$KOH$、$Ca ( OH ) _ {2}$反应均产生氢氧化铜蓝色沉淀,与稀盐酸不反应,不能出现三种明显不同的现象,故不能鉴别;
选项2-项紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,$KOH$、$Ca ( OH ) _ {2}$、稀盐酸三种溶液分别显碱性、碱性、酸性,遇石蕊溶液分别显蓝色、蓝色、红色,不能出现三种明显不同的现象,故不能鉴别;
选项3-项,碳酸钾溶液与稀盐酸反应产生二氧化碳气体,与$Ca ( OH ) _ {2}$反应产生碳酸钙白色沉淀,与氢氧化钾溶液不反应,故分别滴加碳酸钾溶液,产生气泡的是稀盐酸,产生白色沉淀的是$Ca ( OH ) _ {2}$,无明显变化的是$KOH$,故可以鉴别;
选项4-项,无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,$KOH$、$Ca ( OH ) _ {2}$、稀盐酸三种溶液分别显碱性、碱性、酸性,遇酚酞溶液分别显红色、红色、无色,不能出现三种明显不同的现象,故不能鉴别。
5单选题
下列各组物质的溶液,只需组内物质相互反应,就能区别的是()
题目答案
您的答案
答案解析
选项1-项,$Cu ( NO _ {3} ) _ {2}$溶液是蓝色的,首先鉴别出蓝色的$Cu ( NO _ {3} ) _ {2}$溶液,但其余物质的溶液两两混合均没有明显现象故不加其他试剂无法鉴别;选项2-项,$FeCl _ {3}$溶液是黄色的,能与$FeCl _ {3}$溶液反应产生红褐色沉淀的是$NaOH$溶液,再将剩余的两种溶液分别滴加至红褐色沉淀中,能使沉淀消失的是$HNO _ {3}$,无明显变化的是氯化钠溶液,故不加其他试剂可以鉴别;选项3-项,组内四种物质的溶液两两混合时,$BaCl _ {2}$溶液与$K _ {2} SO _ {4}、Na _ {2} CO _ {3}$溶液反应均能产生白色沉淀,但其余物质的溶液两两混合均没有明显现象,故不加其他试剂无法鉴别;选项4-项,$CuCl _ {2}$溶液是蓝色的,首先鉴别出蓝色的$CuCl _ {2}$溶液,$BaCl _ {2}$溶液与$H _ {2} SO _ {4}$反应能产生白色沉淀,但其余物质的溶液两两混合均没有明显现象,故不加其他试剂无法鉴别。