氨气是一种密度比空气小,有刺激性气味的气体.加热条件下,氨气能将氧化铜还原成铜,反应的化学方程式为:2NH$_3$+3CuO$\xlongequal[]{△}$N$_2$+3Cu+3H$_2$O,如图所示,挤压鼓气球把空气鼓入盛有浓氨水的集气瓶中,使氨气进入试管,用酒精灯给试管加热,即可以达到实验目的,关于实验有下列几种说法: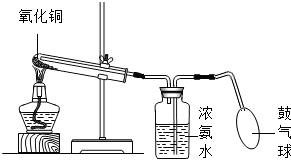
①实验中,试管口应略向下倾斜;
②反应一段时间后可以看到试管内有红色固体生成;
③反应结束后,先撤出导管,再熄灭酒精灯,以免液体倒流;
④装置没有对尾气进行处理,会污染环境.
以上说法正确的是( )
题目答案
您的答案
答案解析
分析:
根据氨气能将氧化铜还原成铜的实验的原理、装置及注意的实行分析有关的说法.
解答:
解:①由于氨气还原氧化铜时有水生成,为防止生成的水倒流引起试管的炸裂,应将试管口应略向下倾斜.故①正确;
②由于氨气还原氧化铜时生成的铜是红色的.所以,反应一段时间后可以看到试管内有红色固体生成.故②正确;
③由装置的特点可知,液体不会倒流.故③不正确;
④反应的尾气含有氨气,会污染环境.所以,装置对尾气进行处理,否则会污染环境.
由以上分析可知,C正确.A、B、D错误.
故选C.
点评:
本题主要考查了氨气还原氧化铜的实验现象、方程式的书写及对装置的评价,了解相关知识是解答的关键.