(多选)将等质量的锌、铁两种金属,同时分别放入两份完全相同的稀盐酸中,充分反应.生成H$_2$的质量与反应时间的关系如图所示.以下结论中,正确的是( )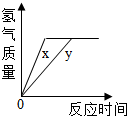
题目答案
您的答案
答案解析
分析:
根据题目的信息可知:因为等质量的锌、铁两种金属,同时分别放入两份完全相同的稀盐酸中,充分反应,生成H$_2$的质量相等,因为生成相同质量的氢气,用的盐酸一样多,所以盐酸一定完全反应;和铁可金属锌能都有剩余,也可能锌恰好完全反应,铁有剩余.在金属的活动性顺序中,锌排在铁的前面,因此锌反应的比铁快.
解答:
解:A、锌排在铁的前面,因此锌反应的比铁快,x、y分别为锌、铁,故选项A错误;
B、充分反应,生成H$_2$的质量相等,因为生成相同质量的氢气,用的盐酸一样多,所以盐酸一定完全反应;故选项B正确;
C、因为生成相同质量的氢气,和铁可金属锌能都有剩余,也可能锌恰好完全反应,故C错;
D、相同质量的情况下,铁产生的氢气比锌多,金属铁一定有剩余,锌可能有剩余,故选项D正确;
故选BD.
点评:
本题考查的是金属的活动性顺序的探究,是近几年来中考考查的重点内容之一.本题型考查实验设计的同时,也考查了学生对实验设计题的评价能力,希望同学们认真把握.