实验室制取CO2的化学方程式为,采用的发生装置和收集装置是(填字母序号)。
题目答案
您的答案
答案解析
碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为$CaCO _ {3} + 2 HCl = CaCl _ {2} + H _ {2} O + CO _ {2} \uparrow$,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,能溶于水,采用的发生装置是B,收集装置是D。
实验室制取CO2的化学方程式为,采用的发生装置和收集装置是(填字母序号)。
碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为$CaCO _ {3} + 2 HCl = CaCl _ {2} + H _ {2} O + CO _ {2} \uparrow$,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,能溶于水,采用的发生装置是B,收集装置是D。
继续加热,观察到黑色粉末中出现红色物质,澄清石灰水逐渐变浑浊。请你写出相关反应的化学方程式:、。
书写化学方程式时应注意反应条件和气体符号及沉淀符号的标注。
取KClO$_3$与MnO$_2$的混合物共35g放入试管中,充分加热后剩余固体的质量为25.4g,冷却至室温后,将该剩余固体溶于适量水中,过滤后得到100g不饱和溶液.往该溶液中滴加AgNO$_3$溶液至恰好不再产生沉淀,共用去130.7g AgNO$_3$溶液.问:
(1)产生O$_2$的质量为g.
(2)生成KCl的质量为g
(3)所得溶液中溶质的质量分数为%.
分析:
(1)根据质量守恒定律可知,固体减少的质量就是生成的氧气的质量;
(2)根据KClO$_3$与MnO$_2$的混合物受热分解的方程式,由氧气的质量可求出生成的氯化钾的质量;
(3)根据氯化钾与硝酸银反应的方程式,由氯化钾的质量可求出生成的硝酸钾、氯化银的质量,再根据质量守恒定律求出生成的溶液的质量,最后求出得溶液中溶质的质量分数.
解答:
解:(1)由质量守恒定律可知,生成的氧气的质量为:35g-25.4g=9.6g;
(2)设生成的氯化钾的质量为x
2KClO$_3$$\xlongequal[△]{MnO$_2$}$2KCl+3O$_2$↑
149 96
x 9.6g
$\frac {149}{96}$=$\frac {x}{9.6g}$
解得:x=14.9g
(3)设生成AgCl和KNO$_3$的质量分别为y、z
KCl+AgNO$_3$═AgCl↓+KNO$_3$
74.5 143.5 101
14.9g y z
$\frac {74.5}{14.9g}$=$\frac {143.5}{y}$=$\frac {101}{z}$
解得:y=28.7g z=20.2g
所得溶液中溶质的质量分数为:$\frac {20.2g}{100g+130.7g-28.7g}$×100%=10%
故答为:(1)9.6;(2)14.9;(3)所得溶液中溶质的质量分数为10%.
点评:
本题主要考查了根据化学方程式的计算,解答时首先要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.
实验室用氯酸钾制取并收集氧气,应选择的发生装置是(填序号),请写出该反应的文字表达式:。

实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,所以发生装置选A,氧气的密度比空气大,不易溶于水,所以收集装置选C或D。
下列反应都能放出二氧化碳气体,试分析判断,会加剧“温室效应”的主要化学反应的是(填序号)。
①$C + O _ {2} \stackrel {点燃} {=} CO _ {2}$
②$CH _ {4} + 2 O _ {2} \stackrel {点燃} {=} CO _ {2} + 2 H _ {2} O$
③$CaCO _ {3} + 2 HCl = CaCl _ {2} + H _ {2} O + CO _ {2} \uparrow$
④石油+氧气$\stackrel{点燃}→$二氧化碳+水
⑤$2 NaHCO _ {3} \stackrel {\triangle} {=} Na _ {2} CO _ {3} + H _ {2} O + CO _ {2} \uparrow$
一种物质受热分解生成三种物质:。
由一种物质受热分解生成三种物质,很容易联想到高锰酸钾制取氧气的反应,反应条件是加热,可直接在等号上方注明“加热”或用“△”表示。
该反应中含氢元素的化合物有种;反应前后化合价发生了变化的元素是(填元素符号)。
该反应中,化合物CH4、H2O中含有氢元素;反应前后化合价发生变化的元素是C和H,C由﹣4价升高到﹢2价,H由﹢1价降低为0价。
猜想和验证:
猜想 | 操作 | 现象 | 结论 |
假设①:焰心气体含二氧化碳 | 在未点燃的细短玻璃管上口 | 假设①不成立 | |
假设②:焰心气体含石蜡蒸气 | 取一较长的细玻璃管用湿冷毛巾包住中部,将玻璃管下端插入焰心,上端试着用火柴点燃 | 假设②成立 | |
取下长玻璃管,打开湿毛巾 |
验证假设①焰心气体含二氧化碳,应选用的药品为澄清石灰水,根据结论假设①不成立,可推出现象应为澄清石灰水不变浑浊;验证假设②焰心气体含石蜡蒸气,根据石蜡蒸气遇冷易凝固成石蜡固体的特点设计了操作,结合实验操作及结论可推出实验现象,用湿冷毛巾包住细玻璃管中部,玻璃管内的石蜡蒸气遇冷在玻璃管中部凝固成白色石蜡固体,由于石蜡蒸气变成了石蜡固体,导管口没有可燃性气体或可燃性气体很少,故用火柴不能点燃。
写出甲烷燃烧的化学方程式:。
甲烷与氧气在点燃的条件下生成二氧化碳和水。
将煤作为燃料,主要是利用碳元素与氧气反应放出的;有时燃气灶或煤炉会产生黑烟,是因为燃料中的碳不能燃烧。
煤作燃料,主要是利用碳与氧气反应放出的热量;有时燃气灶或煤炉会产生黑烟,是因为燃料中的碳不能充分燃烧而产生了单质碳的小颗粒。
B处紫色石蕊溶液变成红色,C处澄清石灰水变浑浊。B处使紫色石蕊溶液变红的物质是;写出C处发生反应的化学方程式:。
B处使紫色石蕊溶液变红的物质是碳酸而非二氧化碳,二氧化碳与水反应生成了碳酸,碳酸使紫色石蕊溶液变成红色;C处通入二氧化碳使澄清石灰水变浑浊,反应的化学方程式为$CO _ {2} + Ca ( OH ) _ {2} = CaCO _ {3} \downarrow + H _ {2} O$。
现有80g质量分数为10%的硝酸钠溶液,试回答下列问题:[br](1)上述硝酸钠溶液中含溶质的质量为g,溶剂的质量为g;[br](2)若向上述溶液中加入20g水,则溶液中溶质质量分数为%;[br](3)若向上述溶液中加入20g硝酸钠,全部溶解后溶液中溶质的质量分数为%;[br](4)若使上述溶液中溶质的质量分数变为5%,则应加水g。
分析:
解答:
点评:
[br]本题难度不大,掌握溶质质量分数的有关计算、溶液稀释前后溶质的质量不变是正确解答本题的关键所在。
实验室选用A装置制取氧气的化学方程式:。
选择发生装置需要考虑的因素是反应物的状态和反应条件。装置A是固固加热型,且试管口有棉花,说明是加热高锰酸钾制氧气,反应的化学方程式为$2KMnO _ {4} \stackrel { \text { △ } } { = } K _ {2} MnO _ {4} + MnO _ {2} + O _ {2} \uparrow$。
除食用碘盐外,我们还可以食用补充碘元素。
根据材料信息可知,除食用碘盐外,我们还可以食用含碘较多的海产品,如海带、海鱼等食物补充碘元素。
包装香烟、糖果的银白色金属是,体现该金属具有良好的性。
铝具有良好的延展性,可用于香烟、糖果等的包装。
小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动:
【査阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬($Cr SO _ {4}$)溶液……
铝是银白色有光泽
实验一
实验方案:
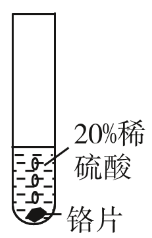
实验现象:铬片表面产生气泡缓慢,溶液变蓝色
结论:铬能与稀硫酸发生反应,反应较慢
实验二
实验方案:
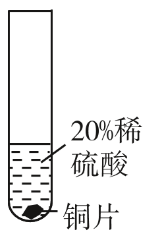
实验现象:
结论:铜不与稀硫酸反应
实验三
实验方案:
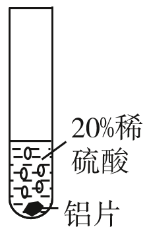
实验现象:铝片表面产生气泡较快
结论:
三种金属在金属活动性顺序中的相对位置关系是(填序号)
【回答问题】(1)用砂纸打磨金属片的目的是。
(2)实验一所发生反应的化学方程式是。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是。(合理答案均可)
【归纳】比较金属活动性强弱的方法有①;②。(合理答案均可)
本题是一道探究金属活动性顺序的实验题,解题时要认真对照实验现象得出正确结论。在实验过程中,由于铜的金属活动性排在氢的后面,故将铜放在稀硫酸中无现象发生,铝片放入稀硫酸中,表面产生气泡较快,说明铝能与稀硫酸反应,根据实验现象可以判断三种金属的金属活动性强弱顺序为AI>Cr>Cu。金属表面的锈迹或污物或氧化物会影响实验的现象,因此实验前应用砂纸打磨金属片。可参照 Fe 与稀硫酸的反应书写Cr与稀硫酸反应的化学方程式。在三种金属中,Cu 的金属活动性最弱,因而 Al 与 Cr 都能与硫酸铜溶液反应,若用$Cu SO _ {4}$溶液代替稀硫酸无法判断 Al 与 Cr 的金属活动性强弱。通过以上实验探究可以得出,比较金属活动性强弱的方法包括:通过金属与酸反应的快慢判断金属活动性强弱或通过金属与另一种金属化合物的溶液反应判断金属活动性强弱。
能源的合理利用与开发是非常重要的。
(1)将煤作为燃料,主要是利用碳与氧气反应放出的;有时燃气灶或煤炉会产生黑烟,是因为燃料中的碳不能燃烧。
(2)汽车用柴油是由加工的产品,汽车尾气中氮的氧化物直接排放到空气中,溶于雨水会形成。
(3)你认为要减少酸雨的产生,可采取的措施有(填序号)。
①减少化石燃料的使用
②把工厂烟囱加高
③燃煤脱硫
(1)煤作燃料,主要是利用碳与氧气反应放出的热量;有时燃气灶或煤炉会产生黑烟,是因为燃料中的碳不能充分燃烧。
(2)汽车尾气中氮的氧化物直接排放到空气中,溶于雨水会形成酸雨。
(3)减少化石燃料的使用、燃煤脱硫均可以减少二氧化硫的排放,可减少酸雨的产生;将工厂烟囱加高并不能减少二氧化硫的排放,不能减少酸雨的产生。
将烧杯迅速倒置,向其中加入少量澄清石灰水,振荡,观察到。
分析:蜡烛燃烧产生的新物质是,蜡烛燃烧为变化。
将烧杯迅速倒置,向其中加入少量澄清石灰水,振荡,澄清石灰水变浑浊,说明生成了二氧化碳,所以蜡烛燃烧属于化学变化。
$Fe _ {2} O _ {3}$中铁元素的质量分数为:。
$Fe _ {2} O _ {3}$中铁元素的质量分数为$\frac {56 \times 2} {56 \times 2 + 16 \times 3} \times 100 \% =$$70 \%$。
根据下列给出的原子结构示意图确定离子符号。

铝离子的符号为,硫离子的符号为。
铝原子最外层电子数为3,易失去3个电子形成铝离子,铝离子的符号为$Al ^ {3 ﹢}$;硫原子最外层电子数为6,易得到2个电子形成硫离子,硫离子的符号为$S ^ {2 -}$。注意书写离子符号时电荷数写在符号右上角,数字在前,“+”“-”在后。