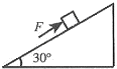
已知力F的一个分力F$_1$跟F成30°角,F$_1$的大小未知,则另一个分力F$_2$的最小值为( )
题目答案
您的答案
答案解析
分析:
已知力F的一个分力F$_1$跟F成30°角,F$_1$的大小未知,根据三角形定则知,当另一个分力与F$_1$垂直时,F$_2$最小.
解答:
解:根据三角形定则知,当另一个分力与F$_1$垂直时,F$_2$最小.如图所示.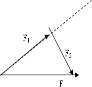 则F$_2$=Fsin30°=$\frac {F}{2}$.故B正确,A、C、D错误.
则F$_2$=Fsin30°=$\frac {F}{2}$.故B正确,A、C、D错误.
故选B.
点评:
解决本题的关键知道三角形的实质和平行四边形的实质是相同的,会根据作图法求出力的最小值.