- 无机化学基础无机化学基础
- 物质的量物质的量
- 物质的量与阿伏伽德罗常数物质的量与阿伏伽德罗常数
- 物质的量浓度物质的量浓度
- 物质的组成性质和分类物质的组成性质和分类
- 离子反应离子反应
- 离子反应 离子方程式离子反应 离子方程式
- 离子共存离子共存
- 氧化还原反应氧化还原反应
- 氧化还原反应的基本概念氧化还原反应的基本概念
- 氧化性和还原性的强弱判断氧化性和还原性的强弱判断
- 氧化还原反应的规律及应用氧化还原反应的规律及应用
- 钠镁铝及其化合物钠镁铝及其化合物
- 钠及其重要化合物钠及其重要化合物
- 碱金属及焰色反应碱金属及焰色反应
- 镁铝及其化合物镁铝及其化合物
- 铝及其化合物的图像和计算铝及其化合物的图像和计算
- 铁铜及其化合物铁铜及其化合物
- 铁及其化合物铁及其化合物
- 铜及其化合物铜及其化合物
- 碳硅及其非金属材料碳硅及其非金属材料
- 碳、硅及其化合物碳、硅及其化合物
- 无机非金属材料无机非金属材料
- 氯及其化合物氯及其化合物
- 氯气氯气
- 氯水、次氯酸及其盐氯水、次氯酸及其盐
- 卤素单质及其化合物的性质卤素单质及其化合物的性质
- 氧硫及其化合物氧硫及其化合物
- 硫及其化合物硫及其化合物
- 氧族元素及臭氧、过氧化性的性质和用途氧族元素及臭氧、过氧化性的性质和用途
- 氮其化合物氮其化合物
- 氮、磷及其化合物氮、磷及其化合物
- 氨气 铵盐氨气 铵盐
- 硝酸及其性质硝酸及其性质
- 化学反应原理化学反应原理
- 原子结构和化学键原子结构和化学键
- 原子结构原子结构
- 化学键化学键
- 元素周期律和元素周期表元素周期律和元素周期表
- 元素周期表元素周期表
- 元素周期律元素周期律
- 化学反应的热效应化学反应的热效应
- 反应热与能量变化的关系反应热与能量变化的关系
- 热化学方程式热化学方程式
- 盖斯定律的应用及反应热的计算盖斯定律的应用及反应热的计算
- 电化学电化学
- 原电池原理原电池原理
- 化学电源化学电源
- 电解原理及其应用电解原理及其应用
- 金属的腐蚀和防护金属的腐蚀和防护
- 化学反应速率化学反应速率
- 化学反应速率化学反应速率
- 化学反应速率的影响因素化学反应速率的影响因素
- 化学平衡化学平衡
- 化学平衡状态化学平衡状态
- 化学平衡常数及转化率的相关计算化学平衡常数及转化率的相关计算
- 化学平衡的移动和化学反应进行的方向化学平衡的移动和化学反应进行的方向
- 弱电解质的电离平衡弱电解质的电离平衡
- 弱电解质的溶解平衡弱电解质的溶解平衡
- 电离平衡常数及其应用电离平衡常数及其应用
- 水的电离和溶液的酸碱性水的电离和溶液的酸碱性
- 水的电离平衡及影响因素水的电离平衡及影响因素
- 溶液的pH及pH的相关计算溶液的pH及pH的相关计算
- 酸碱中和滴定酸碱中和滴定
- 盐类的水解盐类的水解
- 盐类水解及其应用盐类水解及其应用
- 粒子浓度的大小比较粒子浓度的大小比较
- 三大守恒三大守恒
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- Ksp图像及其计算Ksp图像及其计算
- 有机化学与实验操作有机化学与实验操作
- 重要的烃 化石燃料重要的烃 化石燃料
- 同系物和同分异构体同系物和同分异构体
- 化石燃料化石燃料
- 有机物的结构分类与命名有机物的结构分类与命名
- 有机化合物命名有机化合物命名
- 研究有机化合物的步骤和方法研究有机化合物的步骤和方法
- 有机化合物的分类有机化合物的分类
- 烃与卤代烃烃与卤代烃
- 烃的结构与性质烃的结构与性质
- 卤代烃的结构与性质卤代烃的结构与性质
- 烃的含氧衍生物烃的含氧衍生物
- 醇、酚的结构与性质醇、酚的结构与性质
- 醛的结构与性质醛的结构与性质
- 羧酸、酯的结构与性质羧酸、酯的结构与性质
- 高分子化合物 有机合成与推断高分子化合物 有机合成与推断
- 基本营养物质基本营养物质
- 油脂油脂
- 糖类糖类
- 蛋白质蛋白质
- 化学常用仪器和基本操作化学常用仪器和基本操作
- 基本仪器的使用与药品的保存基本仪器的使用与药品的保存
- 基本操作与实验安全基本操作与实验安全
- 物质的检验、分离和提纯物质的检验、分离和提纯
- 物质的检验与鉴别物质的检验与鉴别
- 物质的分离与提纯物质的分离与提纯
- 实验综合探究、设计与评价实验综合探究、设计与评价
- 常见气体的制备实验常见气体的制备实验
- 实验方案的设计与评价实验方案的设计与评价
- 探究性实验探究性实验
- 定量实验之滴定实验定量实验之滴定实验
- 物质的结构与性质物质的结构与性质
- 原子结构与性质原子结构与性质
- 分子结构与性质分子结构与性质
- 晶体结构与性质晶体结构与性质
《氯气》知识速查
氯气的性质
1.氯气的物理性质
颜色 | 气味 | 毒性 | 密度 | 特性 |
黄绿色 | 强烈刺激性气味 | 有毒 | 比空气大 | 易液化 |
[注意] 实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,仅使极少量气体飘进鼻孔。
2.从氯的原子结构认识氯气的化学性质——氧化性

(1)与金属反应:与变价金属反应生成高价金属氯化物。
①与铁反应:2Fe+3Cl2$ \stackrel {点燃} {=} $2FeCl3。
②与铜反应:Cu+Cl2$ \stackrel {点燃} {=} $CuCl2。
(2)与非金属反应
与H2反应:H2+Cl2$ \stackrel {点燃或光照} {=} $2HCl。

与P反应:
Cl2不足:2P+3Cl2(不足)$ \stackrel {点燃} {=} $2PCl3;
Cl2足量:2P+5Cl2(足量)$ \stackrel {点燃} {=} $2PCl5(足量)
(3)与还原性无机化合物反应
①与碘化钾溶液反应:Cl2+2KI=2KCl+I2。
②与SO2水溶液反应:Cl2+SO2+2H2O=H2SO4+2HCl。
③与FeCl2溶液反应:2FeCl2+Cl2=2FeCl3。
3.从化合价的角度认识Cl2的化学性质——歧化反应
氯气与水或碱反应,氯的化合价既有升高又有降低,因而氯气既表现氧化性又表现还原性。
(1)与水反应
氯气与水反应的化学方程式:Cl2+H2O$\rightleftharpoons$HCl+HClO。
(2)与碱(NaOH)反应
反应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O。
[注意]
(1)Cl2具有强氧化性,与变价金属反应时均生成高价态的金属氯化物,如FeCl2不能由两种单质化合而成。
(2)干燥的Cl2没有漂白性,但Cl2能使湿润的有色布条褪色,起漂白作用的是HClO,故不能用pH试纸测量氯水的pH。
(3)1 mol Cl2与强碱完全反应转移电子数为NA,而1 mol Cl2与水充分反应转移电子数小于NA(可逆反应)。
氯气的实验室制法
(一)工业制法——电解法
2NaCl+2H2O$ \stackrel {通电} {=} $2NaOH+H2↑+Cl2↑
(二)实验室制法
1.实验装置
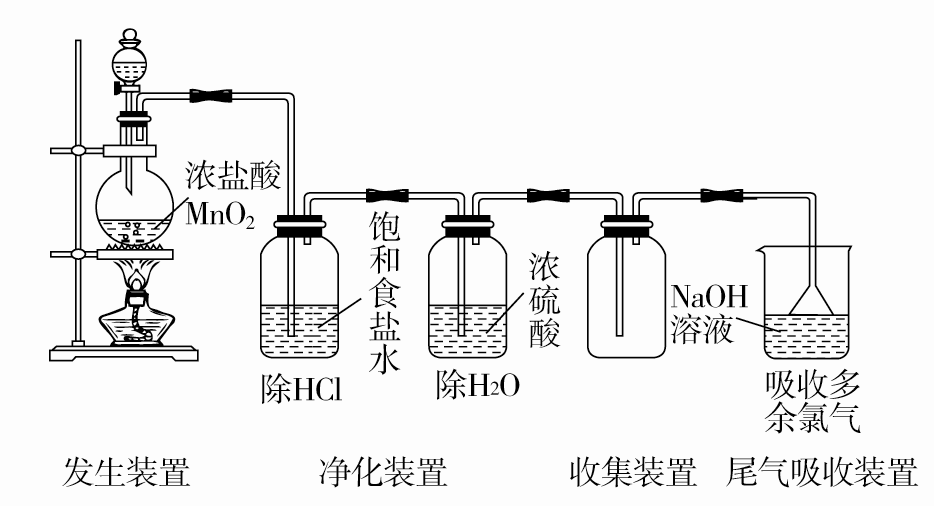
用强氧化剂(如KMnO4、K2Cr2O7、KClO3、MnO2等)氧化浓盐酸也可制氯气:

2.验满方法
(1)将湿润的淀粉碘化钾试纸靠近盛Cl2的瓶口,观察到试纸立即变蓝,则证明已集满。
(2)将湿润的蓝色石蕊试纸靠近盛Cl2的瓶口,观察到试纸先变红后褪色,则证明已集满。
(3)实验室制取Cl2时,也常常根据集气瓶中气体的颜色来判断是否集满。
3.注意事项
(1)反应物的选择:必须用浓盐酸,稀盐酸与MnO2不反应,且随着反应的进行,浓盐酸变为稀盐酸时,反应停止,故盐酸中的HCl不可能全部参加反应。
(2)加热温度:不宜过高,以减少HCl挥发。
(3)尾气吸收:Cl2有毒,必须有尾气吸收装置,常用吸收剂为NaOH溶液或碱石灰,不用澄清石灰水,因澄清石灰水中Ca(OH)2浓度小,吸收慢且吸收不完全。
(4)实验结束后,先排出残留的Cl2,再拆卸装置,避免污染空气。
(5)Cl2在水中的溶解度不大,可不用防倒吸装置。