- 无机化学基础无机化学基础
- 物质的量物质的量
- 物质的量与阿伏伽德罗常数物质的量与阿伏伽德罗常数
- 物质的量浓度物质的量浓度
- 物质的组成性质和分类物质的组成性质和分类
- 离子反应离子反应
- 离子反应 离子方程式离子反应 离子方程式
- 离子共存离子共存
- 氧化还原反应氧化还原反应
- 氧化还原反应的基本概念氧化还原反应的基本概念
- 氧化性和还原性的强弱判断氧化性和还原性的强弱判断
- 氧化还原反应的规律及应用氧化还原反应的规律及应用
- 钠镁铝及其化合物钠镁铝及其化合物
- 钠及其重要化合物钠及其重要化合物
- 碱金属及焰色反应碱金属及焰色反应
- 镁铝及其化合物镁铝及其化合物
- 铝及其化合物的图像和计算铝及其化合物的图像和计算
- 铁铜及其化合物铁铜及其化合物
- 铁及其化合物铁及其化合物
- 铜及其化合物铜及其化合物
- 碳硅及其非金属材料碳硅及其非金属材料
- 碳、硅及其化合物碳、硅及其化合物
- 无机非金属材料无机非金属材料
- 氯及其化合物氯及其化合物
- 氯气氯气
- 氯水、次氯酸及其盐氯水、次氯酸及其盐
- 卤素单质及其化合物的性质卤素单质及其化合物的性质
- 氧硫及其化合物氧硫及其化合物
- 硫及其化合物硫及其化合物
- 氧族元素及臭氧、过氧化性的性质和用途氧族元素及臭氧、过氧化性的性质和用途
- 氮其化合物氮其化合物
- 氮、磷及其化合物氮、磷及其化合物
- 氨气 铵盐氨气 铵盐
- 硝酸及其性质硝酸及其性质
- 化学反应原理化学反应原理
- 原子结构和化学键原子结构和化学键
- 原子结构原子结构
- 化学键化学键
- 元素周期律和元素周期表元素周期律和元素周期表
- 元素周期表元素周期表
- 元素周期律元素周期律
- 化学反应的热效应化学反应的热效应
- 反应热与能量变化的关系反应热与能量变化的关系
- 热化学方程式热化学方程式
- 盖斯定律的应用及反应热的计算盖斯定律的应用及反应热的计算
- 电化学电化学
- 原电池原理原电池原理
- 化学电源化学电源
- 电解原理及其应用电解原理及其应用
- 金属的腐蚀和防护金属的腐蚀和防护
- 化学反应速率化学反应速率
- 化学反应速率化学反应速率
- 化学反应速率的影响因素化学反应速率的影响因素
- 化学平衡化学平衡
- 化学平衡状态化学平衡状态
- 化学平衡常数及转化率的相关计算化学平衡常数及转化率的相关计算
- 化学平衡的移动和化学反应进行的方向化学平衡的移动和化学反应进行的方向
- 弱电解质的电离平衡弱电解质的电离平衡
- 弱电解质的溶解平衡弱电解质的溶解平衡
- 电离平衡常数及其应用电离平衡常数及其应用
- 水的电离和溶液的酸碱性水的电离和溶液的酸碱性
- 水的电离平衡及影响因素水的电离平衡及影响因素
- 溶液的pH及pH的相关计算溶液的pH及pH的相关计算
- 酸碱中和滴定酸碱中和滴定
- 盐类的水解盐类的水解
- 盐类水解及其应用盐类水解及其应用
- 粒子浓度的大小比较粒子浓度的大小比较
- 三大守恒三大守恒
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- Ksp图像及其计算Ksp图像及其计算
- 有机化学与实验操作有机化学与实验操作
- 重要的烃 化石燃料重要的烃 化石燃料
- 同系物和同分异构体同系物和同分异构体
- 化石燃料化石燃料
- 有机物的结构分类与命名有机物的结构分类与命名
- 有机化合物命名有机化合物命名
- 研究有机化合物的步骤和方法研究有机化合物的步骤和方法
- 有机化合物的分类有机化合物的分类
- 烃与卤代烃烃与卤代烃
- 烃的结构与性质烃的结构与性质
- 卤代烃的结构与性质卤代烃的结构与性质
- 烃的含氧衍生物烃的含氧衍生物
- 醇、酚的结构与性质醇、酚的结构与性质
- 醛的结构与性质醛的结构与性质
- 羧酸、酯的结构与性质羧酸、酯的结构与性质
- 高分子化合物 有机合成与推断高分子化合物 有机合成与推断
- 基本营养物质基本营养物质
- 油脂油脂
- 糖类糖类
- 蛋白质蛋白质
- 化学常用仪器和基本操作化学常用仪器和基本操作
- 基本仪器的使用与药品的保存基本仪器的使用与药品的保存
- 基本操作与实验安全基本操作与实验安全
- 物质的检验、分离和提纯物质的检验、分离和提纯
- 物质的检验与鉴别物质的检验与鉴别
- 物质的分离与提纯物质的分离与提纯
- 实验综合探究、设计与评价实验综合探究、设计与评价
- 常见气体的制备实验常见气体的制备实验
- 实验方案的设计与评价实验方案的设计与评价
- 探究性实验探究性实验
- 定量实验之滴定实验定量实验之滴定实验
- 物质的结构与性质物质的结构与性质
- 原子结构与性质原子结构与性质
- 分子结构与性质分子结构与性质
- 晶体结构与性质晶体结构与性质
《物质的分离与提纯》知识速查
.物质分离、提纯的区别与原则
1.物质分离、提纯的区别
(1)物质的分离:将混合物的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯:将混合物中的杂质除去而得到纯净物的过程,又叫混合物的净化或除杂。
2.物质分离、提纯的一般原则
(1)“四原则”:不增(提纯过程中不增加新的杂质);不减(不减少被提纯的物质);易分离(被提纯物质与杂质容易分离);易复原(被提纯物质转化后要易复原)。
(2)“四必须”:除杂试剂必须过量;过量试剂必须除尽(因为过量试剂带入新的杂质);选最佳除杂途径;除去多种杂质时必须考虑加入试剂的顺序。
物质分离与提纯的常用物理方法——常规实验装置
方法、装置 | 适用条件及举例 | 注意事项 |
 | 难溶固体与液体混合物 (例:粗盐提纯时把粗盐溶于水,经过滤把不溶于水的杂质除去) | (1)一贴:滤纸紧贴漏斗内壁;二低:滤纸低于漏斗口,液面低于滤纸边缘;三靠:烧杯紧靠玻璃棒,玻璃棒轻靠三层滤纸处,漏斗下端紧靠烧杯内壁 (2)若一次过滤后滤液仍浑浊,应查找原因后再次过滤 |
1.判断沉淀是否完全的方法:取沉淀后的上层清液少量于试管中,继续加入沉淀剂,若有沉淀产生,说明沉淀不完全,反之说明已经沉淀完全。 2.洗涤沉淀的一般方法:把需要洗涤的沉淀放置在一个干净的过滤器中,向过滤器中加入蒸馏水至浸没沉淀,蒸馏水自然流下,这样反复操作2~3次,直至沉淀洗涤干净。 3.判断沉淀是否洗涤干净的方法:可根据沉淀中可能存在的物质,向最后一次洗涤液中加入适宜的试剂,来检验洗涤程度。 | ||
 | 溶质的溶解度受温度变化影响较小 (例:从NaCl溶液中提取NaCl晶体) | (1)玻璃棒的作用:搅拌,防止液体因局部温度过高造成飞溅 (2)当液体中出现较多固体时,停止加热,用余热蒸干 |
 | (1)萃取:利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液里提取出来 (2)分液:两种液体互不相溶且易分层(例:提取碘水中的I2;分离CCl4和水) | (1)萃取剂应具备的条件: ①萃取剂和原溶剂互不相溶;②溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度 ③萃取剂和溶质不发生反应 (2)分液时下层液体从下口流出,上层液体从上口倒出 (3)萃取分液中的“四步操作”:加萃取剂—振荡放气—静置分层—分液。 |
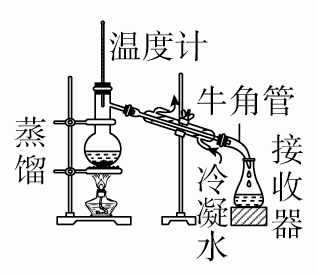 | 两种或两种以上互溶的液体,沸点相差较大 (例:制取蒸馏水,除去水中杂质;石油的分馏) | (1)温度计的水银球应在蒸馏烧瓶支管口处 (2)为防止暴沸,可在蒸馏烧瓶中放几小块沸石或碎瓷片 (3)注意冷凝管水流方向为下进上出 |
 | 杂质气体可溶于某种溶液中而目标气体不溶解 (例:除去Cl2中的HCl气体,可使混合气体通过盛有饱和食盐水的洗气瓶) | (1)从洗气瓶的长导管一端进气 (2)混合物中气体的溶解度差别较大 |
 | 除去胶体中的小分子或离子 (例:除去淀粉胶体中的NaCl) | 要不断更换烧杯中的水或改用流动水,以提高渗析效果 |
 | 利用某些物质在加入某些无机盐时,其溶解度降低而凝聚的性质分离物质 (例:从皂化液中分离肥皂;甘油、蛋白质的盐析) | 盐析后过滤 |
 | 某种含易升华物质的混合物,利用物质升华的性质在加热条件下分离 (例:分离沙子中的碘固体) | |
物质分离与提纯的常用物理方法——创新实验装置
(1)过滤装置的创新——抽滤
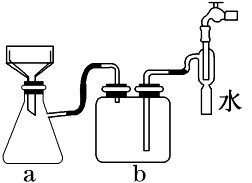 | 由于水流的作用,使装置a、b中气体的压强减小,故使过滤速率加快 |
(2)蒸馏装置的创新
 | 由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器作反应容器,可使反应物能循环利用,提高了反应物的转化率 |
根据物质的物理性质选择分离(提纯)方法
(1)“固+固”混合物的分离(提纯)

(2)“固+液”混合物的分离(提纯)

(3)“液+液”混合物的分离(提纯)

物质分离和提纯常用的化学方法
方法 | 适用条件 | 举例 |
沉淀法 | 在混合物中加入某种试剂,使其中一种以沉淀的形式分离出去 | 加适量AgNO3溶液除去KNO3溶液中的KCl |
转化法 | 不能通过一次反应达到分离的目的时,要先转化为其他物质分离,然后将转化后的物质恢复为原物质 | 分离Fe3+和Al3+时,可加入过量的NaOH溶液,使Fe3+、Al3+分别转化成Fe(OH)3沉淀和NaAlO2溶液,过滤后,分别加入盐酸重新生成Fe3+和Al3+ |
酸碱法 | 被提纯物质不与酸碱反应,而杂质可与酸碱发生反应 | 用盐酸除去SiO2中的石灰石;用NaOH溶液除去铁粉中的铝粉 |
氧化还原法 | ①对混合物中混有的还原性杂质,可加入适当的氧化剂将其氧化为被提纯物质 ②对混合物中混有的氧化性杂质,可加入适当的还原剂将其还原为被提纯物质 | 将过量铁粉加入混有FeCl3的FeCl2溶液中,振荡、过滤,可除去FeCl3杂质 |
加热法 | 混合物中有热稳定性差的物质时,可直接加热,使热稳定性差的物质分解 | 纯碱中混有小苏打 |
调节pH法 | 通过加入试剂来调节溶液的pH,使溶液中杂质成分转化为沉淀而分离 | CaCl2溶液中含有FeCl3杂质,由于Fe3+水解,溶液呈酸性,可加入CaO、Ca(OH)2或CaCO3等调节溶液的pH,将Fe3+转化为沉淀 |
电解法 | 利用电解原理来分离、提纯物质 | 电解精炼铜 |
离子交换法 | 利用离子交换剂来分离、提纯物质 | 软化硬水 |
吸收法 | 常用于气体的净化和干燥,可根据被提纯气体中所含杂质气体的性质,选择适当的固体或溶液作吸收剂。常用装置是洗气瓶或干燥管(U形管) | 如Cl2中混有的HCl气体可通过饱和食盐水除去 |
常见无机物的除杂方法
(括号内为杂质) | 除杂试剂或方法 | 化学方程式或原理 | 分离方法 | |
常 见 固 体 的 除 杂 方 法 | Na2CO3 (NaHCO3) | 加适量NaOH 溶液或加热 | NaHCO3+NaOH=Na2CO3+H2O 2NaHCO3$ \stackrel {\Delta} {=} $Na2CO3+H2O+CO2↑ | — |
NaCl(Na2SO4) | 加适量 BaCl2溶液 | Na2SO4+BaCl2=BaSO4↓+2NaCl | 过滤 | |
NaCl(NH4Cl) | 加热 | NH4Cl$ \stackrel {\Delta} {=} $NH3↑+HCl↑ | — | |
NaCl(MgCl2) | 加适量 NaOH溶液 | MgCl2+2NaOH=Mg(OH)2↓+2NaCl | 过滤 | |
碳粉(CuO) | 稀盐酸 | CuO+2HCl=CuCl2+H2O | 过滤 | |
CuO(Fe) | 磁铁 | — | 吸引 | |
Fe(OH)3胶 体(FeCl3) | 蒸馏水、半透膜 | Fe(OH)3胶体不能通过半透膜 | 渗析 | |
CuS(FeS) | 稀盐酸 | FeS+2HCl=FeCl2+H2S↑ | 过滤 | |
镁粉(铝粉) | 加过量 NaOH溶液 | 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ | 过滤 | |
Fe2O3(Al2O3) | 加过量 NaOH溶液 | Al2O3+2NaOH=2NaAlO2+H2O | 过滤 | |
NH4Cl(FeCl3) | 加适量 氨水 | FeCl3+3NH3·H2O=Fe(OH)3↓+3NH4Cl | 过滤 | |
KNO3(NaCl) | 水 | 根据二者的溶解度随温度的变化不同 | 降温结晶 | |
常 见 液 体 除 杂 | NaHCO3溶液(Na2CO3) | CO2 | Na2CO3+CO2+H2O=2NaHCO3 | 转化法 |
FeCl3溶液 (FeCl2) | Cl2 | 2FeCl2+Cl2=2FeCl3 | 转化法 | |
FeCl3溶液 (CuCl2) | Fe、Cl2 | Fe+CuCl2=Cu+FeCl2 2FeCl2+Cl2=2FeCl3 | 转化法 | |
FeCl2溶液 (FeCl3) | Fe | 2FeCl3+Fe=3FeCl2 | 转化 法 | |
常 见 气 体 除 杂 | H2(NH3) | 浓硫酸 | NH3+H2SO4=NH4HSO4 | 洗气法 |
Cl2(HCl) | 饱和NaCl溶液 | HCl极易溶于水,Cl2在饱和NaCl溶液中的溶解度小 | 洗气法 | |
CO2(HCl) | 饱和NaHCO3溶液 | HCl+NaHCO3=NaCl+H2O+CO2↑ | 洗气法 | |
SO2(HCl) | 饱和NaHSO3溶液 | HCl+NaHSO3=NaCl+H2O+SO2↑ | 洗气法 | |
CO2(SO2) | 饱和NaHCO3溶液 | SO2+2NaHCO3=Na2SO3+H2O+2CO2↑ | 洗气法 | |
CO2(CO) | 灼热CuO | CO+CuO$ \stackrel {\Delta} {=} $Cu+CO2 | 转化法 | |
CO(CO2) | NaOH浓溶液 | CO2+2NaOH=Na2CO3+H2O | 洗气法 | |
N2(O2) | 灼热铜网 | 2Cu+O2$ \stackrel {\Delta} {=} $2CuO | 固定法 |
综合性除杂问题
粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如Ca2+、Mg2+、SO42-等。
要提纯得到纯净的NaCl,可按如下步骤除杂:
首先将粗盐溶于水,再过滤(除去泥沙),然后加入过量的BaCl2溶液,除去Na2SO4;
再加入过量的NaOH溶液,除去MgCl2;然后加入过量的Na2CO3溶液,除去CaCl2和BaCl2;过滤;最后滴加适量盐酸至恰好不再产生气体,除去NaOH和Na2CO3;蒸发溶液,析出NaCl晶体。
BaCl2和NaOH可以互换,但是Na2CO3必须在加入BaCl2之后再加入。滴加适量盐酸必须在过滤操作之后。