- 无机化学基础无机化学基础
- 物质的量物质的量
- 物质的量与阿伏伽德罗常数物质的量与阿伏伽德罗常数
- 物质的量浓度物质的量浓度
- 物质的组成性质和分类物质的组成性质和分类
- 离子反应离子反应
- 离子反应 离子方程式离子反应 离子方程式
- 离子共存离子共存
- 氧化还原反应氧化还原反应
- 氧化还原反应的基本概念氧化还原反应的基本概念
- 氧化性和还原性的强弱判断氧化性和还原性的强弱判断
- 氧化还原反应的规律及应用氧化还原反应的规律及应用
- 钠镁铝及其化合物钠镁铝及其化合物
- 钠及其重要化合物钠及其重要化合物
- 碱金属及焰色反应碱金属及焰色反应
- 镁铝及其化合物镁铝及其化合物
- 铝及其化合物的图像和计算铝及其化合物的图像和计算
- 铁铜及其化合物铁铜及其化合物
- 铁及其化合物铁及其化合物
- 铜及其化合物铜及其化合物
- 碳硅及其非金属材料碳硅及其非金属材料
- 碳、硅及其化合物碳、硅及其化合物
- 无机非金属材料无机非金属材料
- 氯及其化合物氯及其化合物
- 氯气氯气
- 氯水、次氯酸及其盐氯水、次氯酸及其盐
- 卤素单质及其化合物的性质卤素单质及其化合物的性质
- 氧硫及其化合物氧硫及其化合物
- 硫及其化合物硫及其化合物
- 氧族元素及臭氧、过氧化性的性质和用途氧族元素及臭氧、过氧化性的性质和用途
- 氮其化合物氮其化合物
- 氮、磷及其化合物氮、磷及其化合物
- 氨气 铵盐氨气 铵盐
- 硝酸及其性质硝酸及其性质
- 化学反应原理化学反应原理
- 原子结构和化学键原子结构和化学键
- 原子结构原子结构
- 化学键化学键
- 元素周期律和元素周期表元素周期律和元素周期表
- 元素周期表元素周期表
- 元素周期律元素周期律
- 化学反应的热效应化学反应的热效应
- 反应热与能量变化的关系反应热与能量变化的关系
- 热化学方程式热化学方程式
- 盖斯定律的应用及反应热的计算盖斯定律的应用及反应热的计算
- 电化学电化学
- 原电池原理原电池原理
- 化学电源化学电源
- 电解原理及其应用电解原理及其应用
- 金属的腐蚀和防护金属的腐蚀和防护
- 化学反应速率化学反应速率
- 化学反应速率化学反应速率
- 化学反应速率的影响因素化学反应速率的影响因素
- 化学平衡化学平衡
- 化学平衡状态化学平衡状态
- 化学平衡常数及转化率的相关计算化学平衡常数及转化率的相关计算
- 化学平衡的移动和化学反应进行的方向化学平衡的移动和化学反应进行的方向
- 弱电解质的电离平衡弱电解质的电离平衡
- 弱电解质的溶解平衡弱电解质的溶解平衡
- 电离平衡常数及其应用电离平衡常数及其应用
- 水的电离和溶液的酸碱性水的电离和溶液的酸碱性
- 水的电离平衡及影响因素水的电离平衡及影响因素
- 溶液的pH及pH的相关计算溶液的pH及pH的相关计算
- 酸碱中和滴定酸碱中和滴定
- 盐类的水解盐类的水解
- 盐类水解及其应用盐类水解及其应用
- 粒子浓度的大小比较粒子浓度的大小比较
- 三大守恒三大守恒
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- Ksp图像及其计算Ksp图像及其计算
- 有机化学与实验操作有机化学与实验操作
- 重要的烃 化石燃料重要的烃 化石燃料
- 同系物和同分异构体同系物和同分异构体
- 化石燃料化石燃料
- 有机物的结构分类与命名有机物的结构分类与命名
- 有机化合物命名有机化合物命名
- 研究有机化合物的步骤和方法研究有机化合物的步骤和方法
- 有机化合物的分类有机化合物的分类
- 烃与卤代烃烃与卤代烃
- 烃的结构与性质烃的结构与性质
- 卤代烃的结构与性质卤代烃的结构与性质
- 烃的含氧衍生物烃的含氧衍生物
- 醇、酚的结构与性质醇、酚的结构与性质
- 醛的结构与性质醛的结构与性质
- 羧酸、酯的结构与性质羧酸、酯的结构与性质
- 高分子化合物 有机合成与推断高分子化合物 有机合成与推断
- 基本营养物质基本营养物质
- 油脂油脂
- 糖类糖类
- 蛋白质蛋白质
- 化学常用仪器和基本操作化学常用仪器和基本操作
- 基本仪器的使用与药品的保存基本仪器的使用与药品的保存
- 基本操作与实验安全基本操作与实验安全
- 物质的检验、分离和提纯物质的检验、分离和提纯
- 物质的检验与鉴别物质的检验与鉴别
- 物质的分离与提纯物质的分离与提纯
- 实验综合探究、设计与评价实验综合探究、设计与评价
- 常见气体的制备实验常见气体的制备实验
- 实验方案的设计与评价实验方案的设计与评价
- 探究性实验探究性实验
- 定量实验之滴定实验定量实验之滴定实验
- 物质的结构与性质物质的结构与性质
- 原子结构与性质原子结构与性质
- 分子结构与性质分子结构与性质
- 晶体结构与性质晶体结构与性质
《高分子化合物 有机合成与推断》知识速查
有机高分子化合物基本概念
1.单体:能够进行聚合反应形成高分子化合物的低分子化合物。
2.链节:高分子化合物中化学组成相同、可重复的最小单位。
3.聚合度:高分子链中含有链节的数目。如

4.加聚反应:小分子物质以加成反应形式生成高分子化合物的反应,如氯乙烯合成聚氯乙烯的化学方程式为

5.缩聚反应:单体分子间缩合脱去小分子(如H2O、HX等)生成高分子化合物的反应。
如己二酸与乙二醇发生缩聚反应的化学方程式为
 $ \stackrel {催化剂 } {→ } $
$ \stackrel {催化剂 } {→ } $

加聚反应和缩聚反应的常见类型
1.加聚反应的常见类型
(1)一种烯烃单体的聚合反应
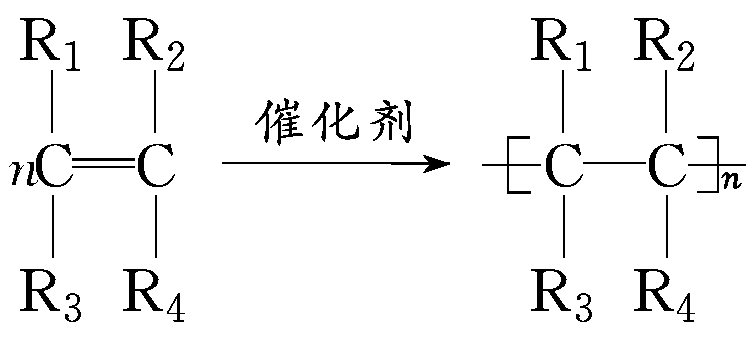
例如,由乙烯聚合得到聚乙烯就属于此反应类型。
(2)一种二烯烃单体的聚合反应

例如,1,3丁二烯的加聚反应就属于此反应类型。

(3)不同烯烃的聚合反应

例如,由乙烯与丙烯聚合得到乙丙橡胶就属于此反应类型。

(4)烯烃和二烯烃的聚合反应

例如,乙烯与1,3丁二烯的共聚反应就属于此反应类型。

(5)碳碳三键的加聚反应

2.常见缩聚反应类型
(1)聚酯类:—OH与—COOH间的缩聚。
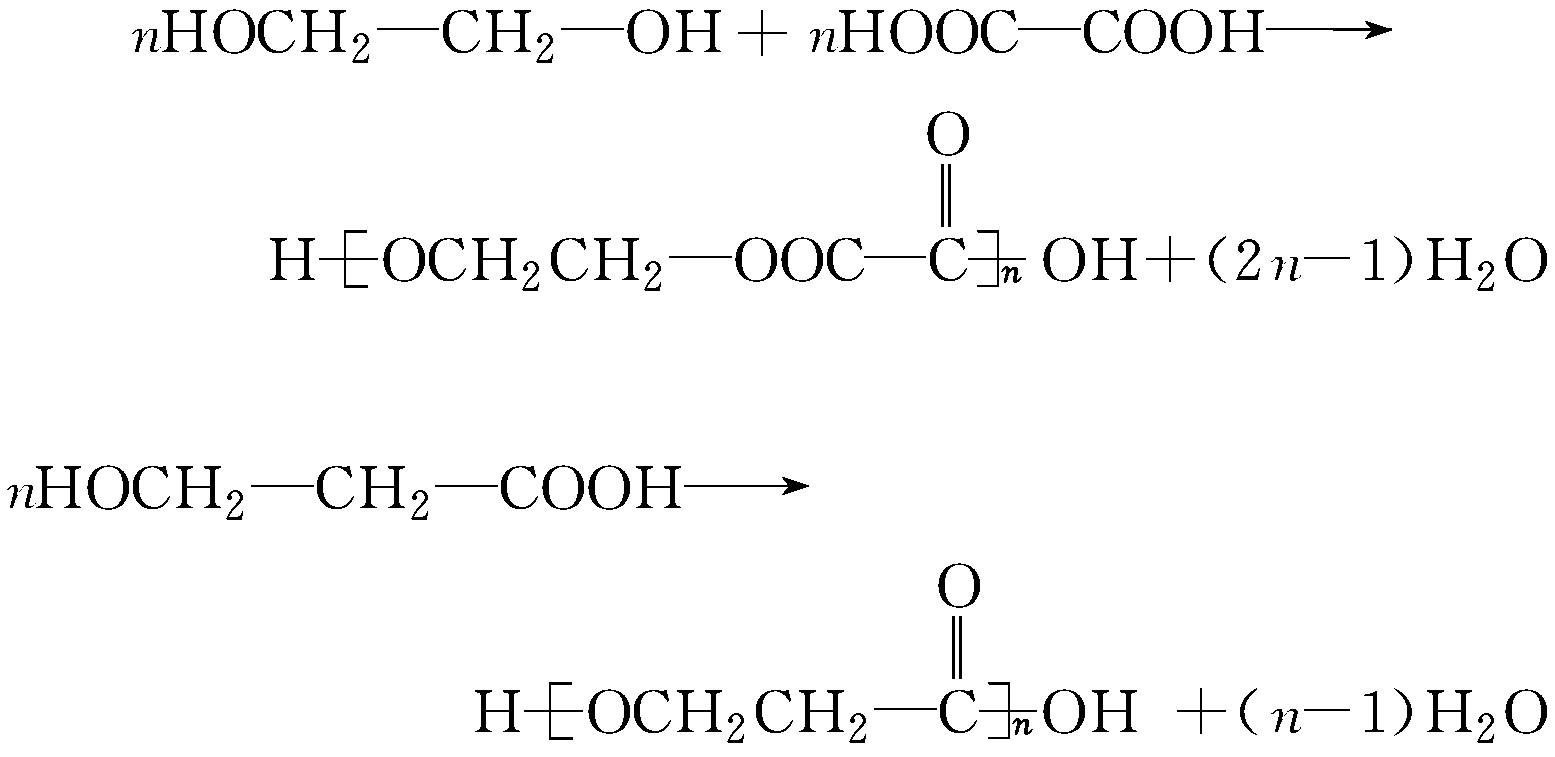
(2)聚氨基酸类:—NH2与—COOH间的缩聚。

(3)酚醛树脂类

由高聚物推导单体的方法与技巧
1.根据特点找单体
(1)加聚反应的特点:
①单体往往是带有双键或三键的不饱和有机物(如乙烯、氯乙烯、甲基丙烯酸、2-甲基-1,3-丁二烯等);
②高分子链节与单体的化学组成相同;
③生成物只有高分子化合物,一般形成线型结构。
(2)缩聚反应的特点:
①单体不一定含有不饱和键,但必须含有两个或两个以上的反应基团(如—OH、—COOH、—NH2、—X等);
②缩聚反应不仅生成高聚物,而且还生成小分子;
③所得高分子化合物的组成跟单体的化学组成不同。
2.简单高分子化合物单体的判断方法

高分子化合物的分类

其中,塑料、合成纤维、合成橡胶又被称为“三大合成材料”。
1.塑料
(1)成分 塑料的主要成分是合成高分子化合物即合成树脂。
(2)分类

①热塑性塑料
加热时变软以至流动,冷却变硬,这种过程是可逆的,可以反复进行。聚乙烯、聚丙烯、聚氯乙烯、聚苯乙烯、聚甲醛,聚碳酸酪,聚酰胺、丙烯酸类塑料等都是热塑性塑料。热塑性塑料中树脂分子链都是线型或带支链的结构,分子链之间无化学键产生,加热时软化流动.冷却变硬的过程是物理变化。
②热固性塑料
第一次加热时可以软化流动,加热到一定温度,产生化学反应固化而变硬,这种变化是不可逆的,此后,再次加热时,已不能再变软流动了。正是借助这种特性进行成型加工,利用第一次加热时的塑化流动,在压力下充满型腔,进而固化成为确定形状和尺寸的制品。这种材料称为热固性塑料。
热固性塑料的树脂固化前是线型或带支链的,固化后分子链之间形成化学键,成为三度的网状结构,不仅不能再熔触,在溶剂中也不能溶解。酚醛树脂、三聚氰胺甲醛、环氧、不饱和聚酯、有机硅等塑料,都是热固性塑料。主要用于隔热、耐磨、绝缘、耐高压电等在恶劣环境中使用的塑料,大部分是热固性塑料,最常用的应该是炒锅把手和高低压电器。
(3)几种常见的塑料
①聚乙烯
高压聚乙烯 | 低压聚乙烯 | |
合成条件 | 150 MPa~300 MPa,170 ℃~200 ℃,引发剂 | 低压、催化剂 |
高分子链 | 较短 | 较长 |
相对分子质量 | 较低 | 较高 |
密度 | 较低 | 较高 |
②酚醛树脂
A.概念:酚醛树脂是用酚类(如苯酚)与醛类(如甲醛)在酸或碱的催化下相互缩合而成的高分子化合物。
B.形成:在酸催化下,等物质的量的甲醛和苯酚反应形成线型结构高分子,其反应为

在碱催化下,等物质的量的甲醛与苯酚或过量的甲醛与苯酚反应生成网状结构的酚醛树脂。
(4)合成高分子化合物的结构
可分为三类:线型结构、支链型结构和网状结构(也称体型结构)。
【注意】
①树脂和塑料不是同种物质,树脂是指没有跟各种添加剂混合的高聚物;塑料是由树脂及增塑剂、稳定剂、着色剂等组成的,其主要成分是树脂。
②甲醛与苯酚在酸催化下形成线型结构,在碱催化下形成网状结构。
2.合成纤维
(1)分类

(2)性能
“六大纶”(涤纶、锦纶、腈纶、丙纶、维纶和氯纶)都具有强度高、弹性好、耐腐蚀、不缩水、质轻保暖等优点,而且还具有各自独特的性能。它们除了改善人们的穿着外,在生产和国防上也有很多用途。如锦纶可制降落伞绳、轮胎帘子线、缆绳和渔网等。
(3)聚酯纤维——涤纶
合成纤维中目前产量占第一位的是聚酯纤维——涤纶。涤纶是聚对苯二甲酸乙二醇酯纤维的商品名。其合成反应为


【注意】
①人造纤维只是将天然纤维加工处理制得,不是合成高分子化合物;合成纤维是以石油、天然气为原料人工合成的高分子化合物。
②维纶具有较好的吸湿性,是因为其分子链上含有羟基。
3.合成橡胶
(1)橡胶的分类
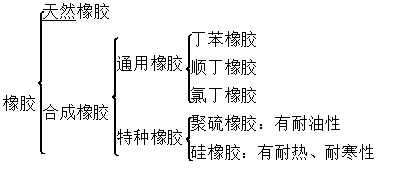
(2)合成橡胶
①原料:以石油、天然气中的二烯烃和烯烃为原料。
②性能:具有高弹性、绝缘性、气密性、耐高温或耐低温等性能。
(3)合成橡胶的合成过程(以顺丁橡胶为例)
①主要原料:1,3丁二烯
②合成原理:nH2C=CH—CH=CH2$ \stackrel {催化剂 } {→ } $ 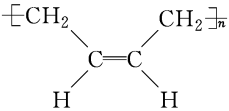 )
)
在催化剂存在下,1,3丁二烯得到以顺式结构为主的聚1,3丁二烯。
顺式聚1,3丁二烯与硫磺等硫化剂混炼即得到顺丁橡胶。硫化剂的作用是打开顺式聚1,3丁二烯的双键,以—S—S—键将顺丁橡胶的线型结构连接为网状结构,得到既有弹性、强度又大的橡胶,但交联程度不宜过大,否则会失去弹性。
4.功能高分子材料和复合材料
(1)功能高分子材料
①含义
功能高分子材料是指既有传统高分子材料的机械性能,又有某些特殊功能的高分子材料。
②分类
A.新型骨架结构的高分子材料。
B.特殊功能材料,即在合成高分子的主链或支链上引入某种功能原子团,使其显示出在光、电、磁、声、热、化学、生物、医学等方面的特殊功能。
③高吸水性树脂
A.合成方法:
a.对淀粉、纤维素等天然吸水材料进行改性,在它们的高分子链上再接上含强亲水性原子团的支链,以提高它们的吸水能力。
b.以带有强亲水性原子团的化合物为单体,均聚或共聚得到亲水性高聚物。
B.性能:
可吸收几百至几千倍于自身质量的水,同时保水能力强,还能耐一定的挤压作用。
C.应用:
干旱地区用于农业、林业、植树造林时抗旱保水,改良土壤,改造沙漠。
(2)复合材料
①含义:指将几种不同的材料组合在一起制成的一种新型材料。其中一种材料作为基体,其他材料作为增强材料。高分子、金属、陶瓷等都可作为基体,目前发展最快的是碳纤维作增强剂。
②性能:
具有强度高、质量轻、耐高温、耐腐蚀等优异性能,弥补了单一材料在性能上的缺陷。
③应用:宇宙航空工业、汽车工业、机械工业、体育用品、人类健康等方面。
【注意】
(1)新型高分子材料与传统合成材料在本质上没有区别,二者重要区别在功能和性能上,新型高分子材料的性能更优异。
(2)复合材料是由两种或多种材料合成的性能优异的材料,不一定是高分子材料。
有机合成
(一)理清有机合成的任务、原则
1.有机合成的任务

2.有机合成的原则
(1)起始原料要廉价、易得、低毒性、低污染。
(2)应尽量选择步骤最少的合成路线。
(3)原子经济性高,具有较高的产率。
(4)有机合成反应要操作简单、条件温和、能耗低、易于实现。
(二)熟记有机合成中官能团的转化
1.官能团的引入
引入官能团 | 引入方法 |
卤素原子 | ①烃、酚的取代; ②不饱和烃与HX、X2的加成; ③醇与氢卤酸(HX)的取代 |
羟基 | ①烯烃与水的加成; ②醛酮与氢气的加成; ③卤代烃在碱性条件下的水解; ④酯的水解 ⑤葡萄糖发酵产生乙醇 |
碳碳双键 | ①某些醇或卤代烃的消去; ②炔烃不完全加成; ③烷烃裂化 |
碳氧双键 | ①醇的催化氧化; ②连在同一个碳上的两个羟基脱水; ③含碳碳三键的物质与水加成 |
羧基 | ①醛基的氧化; ②酯、肽、蛋白质、羧酸盐的水解 |
2.官能团的消除
①通过加成反应可以消除不饱和键(双键、三键)和苯环;
②通过消去、氧化或酯化反应等消除羟基;
③通过加成或氧化反应等消除醛基;
④通过水解反应消除酯基、肽键、卤素原子。
3.官能团的改变
①利用官能团的衍生关系进行衍变,如
R—CH2OH$ \stackrel {O_{2}} {→ } $R—CHO$ \stackrel {O_{2}} {→ } $R—COOH。
②通过某种化学途径使一个官能团变为两个,如
CH3CH2OH$ \stackrel {消去} {→ } $ CH2=CH2$ \stackrel {加成} {→ } $
ClCH2—CH2Cl$ \stackrel {水解} {→ } $ HOCH2—CH2OH。
③通过某种手段改变官能团的位置,如

(三)有机合成中碳骨架的构建
1.链增长的反应
①加聚反应;②缩聚反应;③酯化反应;④利用题目信息所给的反应,如卤代烃的取代反应,醛酮的加成反应……
2.链减短的反应
①烷烃的裂化反应;②酯类、糖类、蛋白质等的水解反应;③利用题目信息所给的反应,如烯烃、炔烃的氧化反应,羧酸及其盐的脱羧反应。
3.常见由链成环的方法
①二元醇成环:
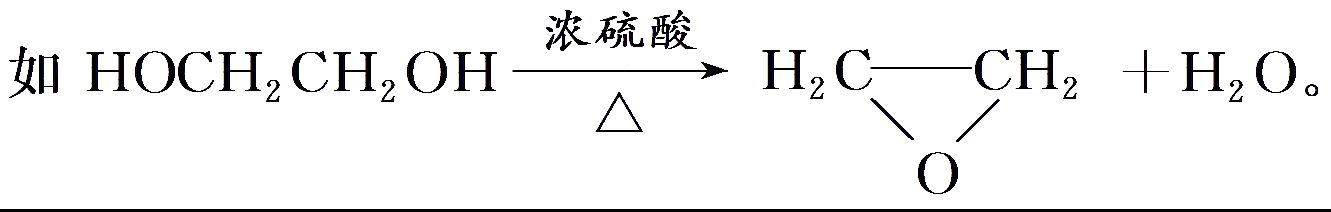
②羟基酸酯化成环:
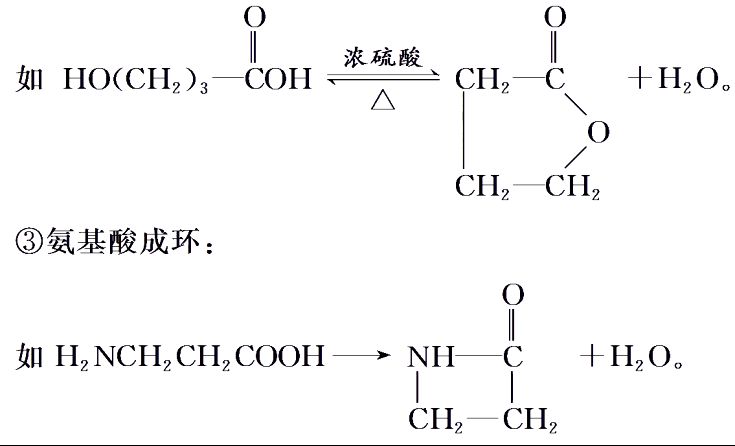
④二元羧酸成环:

(四)明晰有机合成题的解题思路
(五)熟记中学常见的有机合成路线
1.一元合成路线
R—CH=CH2$ \stackrel {HX} {→ } $卤代烃$ \stackrel {NaOH,H_{2}O} {→ } $一元醇$ \stackrel {氧化} {→ } $一元醛$ \stackrel {氧化} {→ } $一元羧酸→酯
2.二元合成路线
CH2=CH2$ \stackrel {X_{2}} {→ } $XCH2—CH2X$ \stackrel {NaOH,H_{2}O} {→ } $二元醇$ \stackrel {氧化} {→ } $二元醛$ \stackrel {氧化} {→ } $二元羧酸→高聚酯(环酯)
3.芳香化合物合成路线

有机合成与推断题的突破
有机推断与有机合成综合题是考查有机化学知识的主流题型,为高考必考题,常以框图题形式出现,解题的关键是找出解题的突破口,一般采用“由特征反应推知官能团的种类,由反应机理推知官能团的位置,由转化关系和产物结构推知碳架结构,再综合分析验证,最终确定有机物结构”的思路求解。
(一)从有机物的特殊结构、性质进行解题
1.根据有机物的特殊反应确定分子中的官能团
官能团种类 | 试剂与条件 | 判断依据 |
碳碳双键或碳碳三键 | 溴水 | 橙红色褪去 |
酸性KMnO4溶液 | 紫红色褪去 | |
卤素原子 | NaOH溶液,加热,AgNO3溶液和稀硝酸 | 有沉淀产生 |
醇羟基 | 钠 | 有H2放出 |
酚羟基 | FeCl3溶液 | 显紫色 |
浓溴水 | 有白色沉淀产生 | |
羧基 | NaHCO3溶液 | 有CO2气体放出 |
醛基 | 银氨溶液,水浴加热 | 有银镜生成 |
新制Cu(OH)2悬浊液,煮沸 | 有砖红色沉淀生成 | |
酯基 | NaOH与酚酞的混合液,加热 | 红色褪去 |
2.由官能团的特殊结构确定有机物的类别
(1)羟基连在脂肪烃基或苯环侧链上的物质为醇,而直接连在苯环上的物质为酚。
(2)与连接醇羟基(或卤素原子)碳原子相邻的碳原子上没有氢原子,则不能发生消去反应。
(3)—CH2OH氧化生成醛,进一步氧化生成羧酸; 氧化生成酮。
氧化生成酮。
(4)1 mol —COOH与NaHCO3反应时生成1 mol CO2。
3.根据特定的反应条件推断
(1)“光照,”是烷烃和烷基中的氢原子被卤素原子取代的反应条件,如①烷烃的取代;②芳香烃及其他芳香族化合物侧链烷基的取代;③不饱和烃中烷基的取代。
(2)“$\underset {\Delta} {\stackrel {Ni} {→ }}$”为不饱和键加氢反应的条件,包括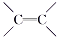 、
、 与H2的加成。
与H2的加成。
(3)“$\underset {\Delta} {\stackrel {浓H_{2}SO_{4}} {→ }}$”是①醇消去H2O生成烯烃或炔烃;②酯化反应;③醇分子间脱水生成醚的反应;④纤维素的水解反应。
(4)“$\underset {\Delta} {\stackrel {NaOH醇溶液} {→ }}$”或“$\underset {\Delta} {\stackrel {浓NaOH醇溶液} {→ }}$”是卤代烃消去HX生成不饱和有机物的反应条件。
(5)“$\underset {\Delta} {\stackrel {NaOH水溶液} {→ }}$”是①卤代烃水解生成醇;②酯类水解反应的条件。
(6)“$\underset {\Delta} {\stackrel {稀H_{2}SO_{4}} {→ }}$”是①酯类水解;②糖类水解;③油脂的酸性水解;④淀粉水解的反应条件。
(7)“$\underset {\Delta} {\stackrel {Cu或Ag} {→ }}$”“$ \stackrel {[O]} {→ } $”为醇氧化的条件。
(8)“$ \stackrel {Fe} {→ } $”为苯及其同系物苯环上的氢原子被卤素原子取代的反应条件。
(9)溴水或Br2的CCl4溶液是不饱和烃加成反应的条件。
(10)“$\underset {银氨溶液 } {\stackrel {O_{2}、新制Cu(OH)_{2}} {→ }}$”“$ \stackrel {【O】} {→ } $”是醛氧化的条件。
4.根据有机反应中定量关系推断
(1)烃和卤素单质的取代:取代1 mol 氢原子,消耗1 mol 卤素单质(X2)。
(2) 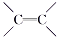 的加成:与H2、Br2、HCl、H2O等加成时按物质的量比1∶1加成。
的加成:与H2、Br2、HCl、H2O等加成时按物质的量比1∶1加成。
(3)含—OH有机物与Na反应时:2 mol —OH生成1 mol H2。
(4)1 mol —CHO对应2 mol Ag;或1 mol —CHO对应1 mol Cu2O。
(5)物质转化过程中相对分子质量的变化:
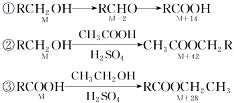
(关系式中M代表第一种有机物的相对分子质量)