- 无机化学基础无机化学基础
- 物质的量物质的量
- 物质的量与阿伏伽德罗常数物质的量与阿伏伽德罗常数
- 物质的量浓度物质的量浓度
- 物质的组成性质和分类物质的组成性质和分类
- 离子反应离子反应
- 离子反应 离子方程式离子反应 离子方程式
- 离子共存离子共存
- 氧化还原反应氧化还原反应
- 氧化还原反应的基本概念氧化还原反应的基本概念
- 氧化性和还原性的强弱判断氧化性和还原性的强弱判断
- 氧化还原反应的规律及应用氧化还原反应的规律及应用
- 钠镁铝及其化合物钠镁铝及其化合物
- 钠及其重要化合物钠及其重要化合物
- 碱金属及焰色反应碱金属及焰色反应
- 镁铝及其化合物镁铝及其化合物
- 铝及其化合物的图像和计算铝及其化合物的图像和计算
- 铁铜及其化合物铁铜及其化合物
- 铁及其化合物铁及其化合物
- 铜及其化合物铜及其化合物
- 碳硅及其非金属材料碳硅及其非金属材料
- 碳、硅及其化合物碳、硅及其化合物
- 无机非金属材料无机非金属材料
- 氯及其化合物氯及其化合物
- 氯气氯气
- 氯水、次氯酸及其盐氯水、次氯酸及其盐
- 卤素单质及其化合物的性质卤素单质及其化合物的性质
- 氧硫及其化合物氧硫及其化合物
- 硫及其化合物硫及其化合物
- 氧族元素及臭氧、过氧化性的性质和用途氧族元素及臭氧、过氧化性的性质和用途
- 氮其化合物氮其化合物
- 氮、磷及其化合物氮、磷及其化合物
- 氨气 铵盐氨气 铵盐
- 硝酸及其性质硝酸及其性质
- 化学反应原理化学反应原理
- 原子结构和化学键原子结构和化学键
- 原子结构原子结构
- 化学键化学键
- 元素周期律和元素周期表元素周期律和元素周期表
- 元素周期表元素周期表
- 元素周期律元素周期律
- 化学反应的热效应化学反应的热效应
- 反应热与能量变化的关系反应热与能量变化的关系
- 热化学方程式热化学方程式
- 盖斯定律的应用及反应热的计算盖斯定律的应用及反应热的计算
- 电化学电化学
- 原电池原理原电池原理
- 化学电源化学电源
- 电解原理及其应用电解原理及其应用
- 金属的腐蚀和防护金属的腐蚀和防护
- 化学反应速率化学反应速率
- 化学反应速率化学反应速率
- 化学反应速率的影响因素化学反应速率的影响因素
- 化学平衡化学平衡
- 化学平衡状态化学平衡状态
- 化学平衡常数及转化率的相关计算化学平衡常数及转化率的相关计算
- 化学平衡的移动和化学反应进行的方向化学平衡的移动和化学反应进行的方向
- 弱电解质的电离平衡弱电解质的电离平衡
- 弱电解质的溶解平衡弱电解质的溶解平衡
- 电离平衡常数及其应用电离平衡常数及其应用
- 水的电离和溶液的酸碱性水的电离和溶液的酸碱性
- 水的电离平衡及影响因素水的电离平衡及影响因素
- 溶液的pH及pH的相关计算溶液的pH及pH的相关计算
- 酸碱中和滴定酸碱中和滴定
- 盐类的水解盐类的水解
- 盐类水解及其应用盐类水解及其应用
- 粒子浓度的大小比较粒子浓度的大小比较
- 三大守恒三大守恒
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- 难溶电解质的溶解平衡难溶电解质的溶解平衡
- Ksp图像及其计算Ksp图像及其计算
- 有机化学与实验操作有机化学与实验操作
- 重要的烃 化石燃料重要的烃 化石燃料
- 同系物和同分异构体同系物和同分异构体
- 化石燃料化石燃料
- 有机物的结构分类与命名有机物的结构分类与命名
- 有机化合物命名有机化合物命名
- 研究有机化合物的步骤和方法研究有机化合物的步骤和方法
- 有机化合物的分类有机化合物的分类
- 烃与卤代烃烃与卤代烃
- 烃的结构与性质烃的结构与性质
- 卤代烃的结构与性质卤代烃的结构与性质
- 烃的含氧衍生物烃的含氧衍生物
- 醇、酚的结构与性质醇、酚的结构与性质
- 醛的结构与性质醛的结构与性质
- 羧酸、酯的结构与性质羧酸、酯的结构与性质
- 高分子化合物 有机合成与推断高分子化合物 有机合成与推断
- 基本营养物质基本营养物质
- 油脂油脂
- 糖类糖类
- 蛋白质蛋白质
- 化学常用仪器和基本操作化学常用仪器和基本操作
- 基本仪器的使用与药品的保存基本仪器的使用与药品的保存
- 基本操作与实验安全基本操作与实验安全
- 物质的检验、分离和提纯物质的检验、分离和提纯
- 物质的检验与鉴别物质的检验与鉴别
- 物质的分离与提纯物质的分离与提纯
- 实验综合探究、设计与评价实验综合探究、设计与评价
- 常见气体的制备实验常见气体的制备实验
- 实验方案的设计与评价实验方案的设计与评价
- 探究性实验探究性实验
- 定量实验之滴定实验定量实验之滴定实验
- 物质的结构与性质物质的结构与性质
- 原子结构与性质原子结构与性质
- 分子结构与性质分子结构与性质
- 晶体结构与性质晶体结构与性质
《基本操作与实验安全》知识速查
药品的取用
①取用粉末状或小颗粒状固体用药匙,若药匙不能伸入试管,可用纸槽,要把药品送入试管底部,而不能沾在管口和管壁上。块状和大颗粒固体用镊子夹取。
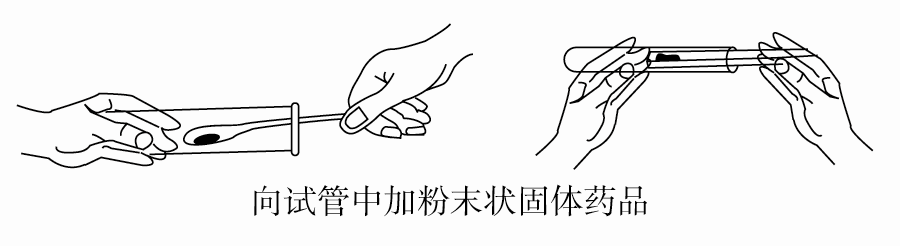
②取少量液体可用胶头滴管。取用较多的液体用倾倒法,注意试剂瓶上的标签向手心。向容量瓶、漏斗中倾倒液体时,要用玻璃棒引流。

试纸的使用
试纸 种类 | 应用 | 使用方法 | 注意 |
石蕊试纸 | 检验酸碱性(定性) | ①检验液体:取一小块试纸放在洁净干燥的表面皿或玻璃板上,用洁净干燥的玻璃棒蘸取待测液点在试纸的中部,观察颜色变化 ②检验气体:一般先用蒸馏水把试纸润湿,粘在玻璃棒的一端,并使之接近容器口,观察颜色变化 | ①试纸不可伸入溶液中,也不能与管口接触 ②测溶液pH时,pH试纸不能先润湿,因为润湿相当于将原溶液稀释了 |
pH试纸 | 检验酸碱性强弱(定量) | ||
品红试纸 | 检验SO2等具有漂白性的物质 | ||
KI淀粉试纸 | 检验Cl2等具有氧化性的物质 |
仪器的洗涤
①洗净的标准:内壁附着均匀水膜,不凝聚成水滴,也不成股流下。
②常见残留物的洗涤
待清洗仪器 | 污物 | 清洗试剂 |
做过KMnO4分解实验的试管 | MnO2 | 浓盐酸 |
做过碘升华的烧杯 | 碘 | 酒精 |
待清洗仪器 | 污物 | 清洗试剂 |
长期存放FeCl3溶液的试剂瓶 | Fe(OH)3 | 稀盐酸 |
长期存放澄清石灰水的试剂瓶 | CaCO3 | 稀盐酸 |
做过银镜实验的试管 | 银 | 稀硝酸 |
做过油脂实验的试管 | 油污 | NaOH或热纯碱溶液 |
做过硫实验的试管 | 硫 | 二硫化碳 |
做过苯酚实验的烧瓶 | 苯酚 | NaOH或酒精 |
气密性的检验
①装置气密性检查必须是在放入药品之前进行。
②常见气密性检查方法
简答题应注意答题规范,对装置气密性的检查可按如下文字进行答题:
装置形成封闭体系→操作(微热、手捂、热毛巾捂、加水等)→描述现象→得出结论。
方法 | 微热法 | 液差法(1) | 液差法(2) | 气压法 | 外压法 |
原理 | 升高装置中气体的温度,使气体膨胀 | 缩小装置中气体的体积,增大压强 | 缩小装置中气体的体积,增大压强 | 封闭气体的压强增大,使液滴不能滴下 | 增压或减压使出现液柱或产生气泡 |
图示 | 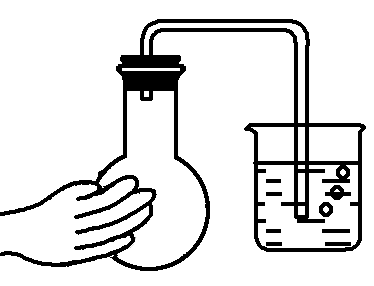 | 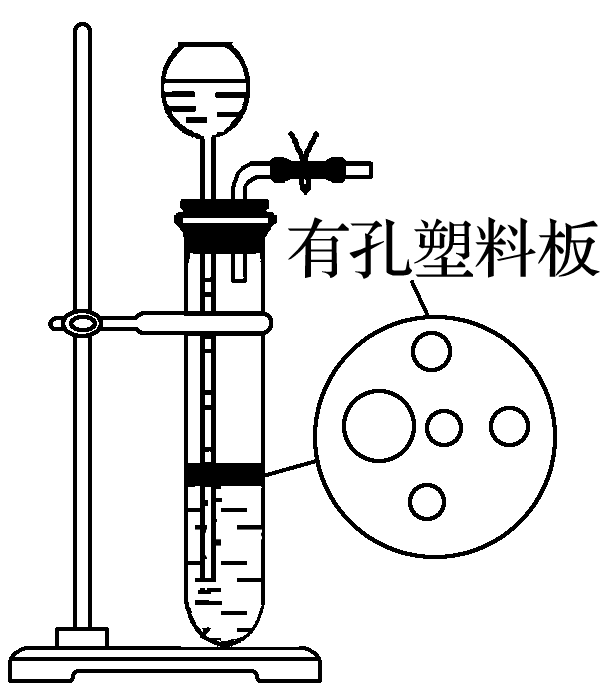 | 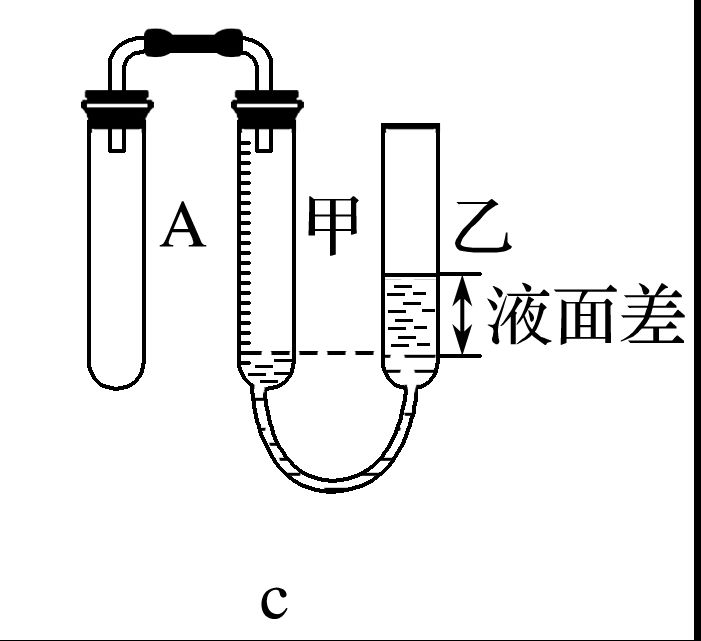 | 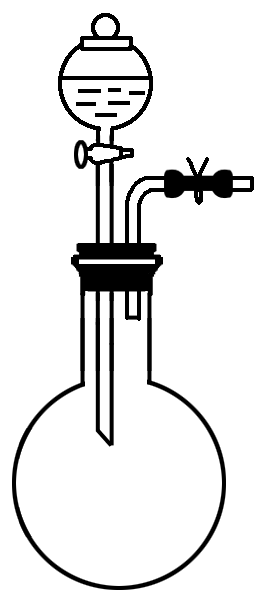 | 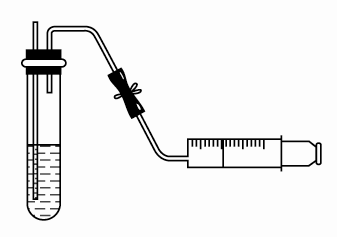 |
具体操作 | 塞紧橡胶塞,将导气管末端伸入盛水的烧杯中,用手捂热(或用酒精灯微热)烧瓶 | 塞紧橡胶塞,用止水夹夹住导气管的橡胶管部分,从长颈漏斗向试管中注水 | 塞紧橡胶塞,往乙管中注水,出现液面差停止加水 | 塞紧橡胶塞,关闭止水夹,打开分液漏斗活塞,向烧瓶中加水 | 塞紧橡胶塞,打开止水夹推动或拉动注射器 |
现象说明 | 烧杯中有气泡产生,停止微热,冷却后导气管末端形成一段水柱,且保持一段时间不下降,说明气密性良好。 | 停止加水后,长颈漏斗中的液面高于试管中的液面,且液面差不再改变,说明气密性良好。 | 停一段时间后乙管液面差不再改变,说明气密性良好。 | 一段时间后,液滴不能滴下,说明气密性良好。 | 推动注射器之后导管中出现一段液柱,且液面差不改变,拉动注射器试管中产生气泡,说明气密性良好。 |
物质的溶解
①固体物质的溶解
一般在烧杯或试管中进行,为了加速溶解,常采用搅拌、粉碎、振荡或加热等措施,但FeCl3、AlCl3等易水解的固体溶解时不能加热。
②气体物质的溶解
a.对于溶解度较小的气体(如Cl2等),为了增大气体分子与水分子的接触,应将导管插入水中(如图A)。
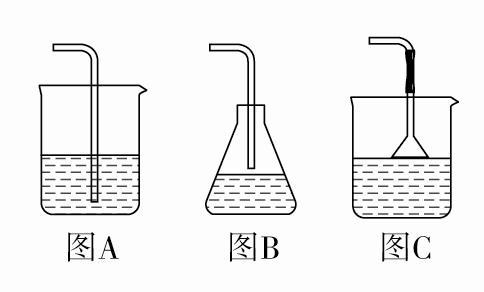
b.对于极易溶于水的气体(如NH3、HCl等),导管口只能靠近液面,最好在导管口连接一倒置的漏斗,并使漏斗边缘刚好贴近液面,这样可以增大气体的吸收率,减少气体的逸出,同时也可避免出现液体的倒吸(如图B和图C)。
③液体物质的溶解
当用水溶解密度比水大的液体时,一般把溶质注入水中溶解;当溶解密度比水小的液体时,一般把水注入溶质中溶解。
常见危险化学药品的标志

化学实验常见事故的处理方法
意外事故 | 处理方法 |
创伤 | 用药棉清理伤口,用双氧水擦洗,轻伤可以涂紫药水(或红汞、碘酒),用创可贴外敷或用绷带包扎 |
烫伤和烧伤 | 用药棉浸90%~95%酒精轻涂伤处,再涂烫伤药膏 |
眼睛灼伤 | 用大量水冲洗,边洗边眨眼。若为碱灼伤,再用2%硼酸溶液淋洗;若为酸灼伤,再用3%NaHCO3溶液淋洗 |
浓硫酸洒在皮肤上 | 皮肤上不慎洒上浓硫酸,先用干布擦去,再用大量的水冲洗,最后涂上3%~5%NaHCO3溶液 |
碱洒在皮肤上 | 用较大量水冲洗,再涂上硼酸溶液 |
溴腐蚀受伤 | 先用苯或甘油洗伤口,再用水洗 |
苯酚洒在皮肤上 | 迅速用酒精洗 |
磷灼伤 | 用1%的AgNO3、5%的CuSO4或浓KMnO4溶液冲洗伤口,然后包扎 |
吸入刺激性或有毒气体 | 吸入Cl2、HCl时,可吸入少量酒精和乙醚的混合蒸气解毒。吸入H2S或CO气体而感到不适时,应立即到室外呼吸新鲜空气。氨气、溴中毒时不可进行人工呼吸 |
毒物进入口内 | 将5~10 mL稀硫酸铜溶液加入一杯温水中,内服后,将手指伸入咽喉部,促使呕吐,吐出毒物后立即送医院 |
触电 | 首先切断电源,然后必要时进行人工呼吸 |
起火 | 起火后要立即一面灭火,一面防止火势蔓延。一般酒精及有机物燃烧,小面积起火,应迅速用湿布、石棉布或沙子盖灭,钠、磷着火用沙土盖灭;火势较大时可使用泡沫灭火器(但电器设备引起的火灾不能使用泡沫灭火器,只能使用二氧化碳或四氯化碳灭火器灭火)。若衣服着火,则应迅速脱下衣服或用石棉布覆盖着火处 |
水银洒在桌面上 | 若摔破温度计,应立即在水银上撒上硫粉进行处理(Hg+S=HgS) |
实验安全十防范
①防爆炸:点燃可燃气体(如H2、CO、CH4、C2H2、C2H4)前要先验纯,用CO、H2还原Fe2O3、CuO之前,除要检验气体纯度外,还要向试管中先通一会儿气体排除装置中空气。
②防暴沸:稀释浓H2SO4或将浓H2SO4与酒精混合时,要将密度大的浓H2SO4缓慢倒入水或酒精中;加热液体混合物时要加沸石(或碎瓷片)。
③防失火:实验室中的可燃物一定要远离火源(如制取乙醚时,乙醚离酒精灯要尽可能地远些)。
④防倒吸:加热法制取气体并用排水法收集气体实验结束时,要先撤导管后熄灭酒精灯;或吸收溶解度较大的气体时,要加装安全瓶,通常安全瓶有以下三种:
a.隔离式。原理:导气管末端与易溶气体的液体呈隔离状态。例如制取溴苯的实验中设置了隔离式Ⅰ来吸收HBr,吸收NH3或HCl时可用隔离式Ⅲ。
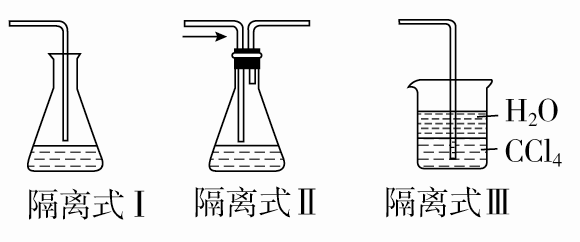
b.肚容式。原理:由于上部有一容积较大的空间,当水进入该部分时,烧杯(或试管)中液面显著下降而低于漏斗口(或导管口),由于重力作用,液体又流回到烧杯(或试管)中。例如制取NH3实验中设置了这一装置来吸收NH3尾气。
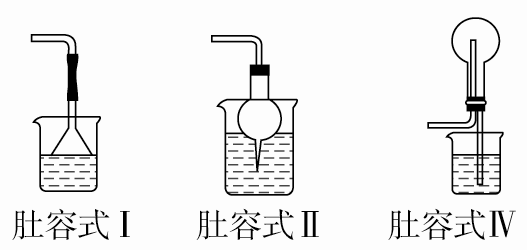
c.接收式。原理:使用较大容积的容器将可能倒吸来的液体接收,防止进入前端装置(如气体发生装置等)。它与肚容式的主要区别是液体不再流回到原容器。
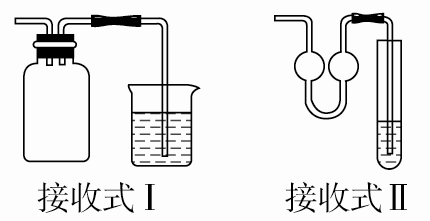
⑤防污染:制取有毒气体(如CO、SO2、H2S、Cl2、NO、NO2等)时,应在通风橱中进行,并安装以下处理装置:
a.燃烧式。原理:有毒可燃性气体(如CO)被燃烧除去。
b.吸收式。原理:有毒气体如Cl2、SO2、H2S等与碱反应被除去。
c.收集式。原理:用气囊将有害气体收集起来,另作处理。
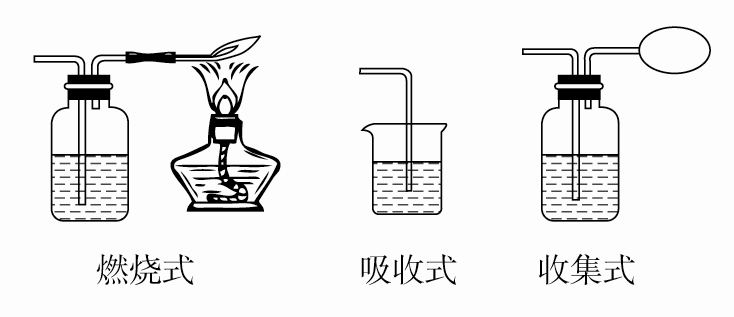
⑥防堵塞:防止堵塞导管,或使液体顺利通入,或使内外压强相等。
a.液封式。原理:流动的气体若在前方受阻,锥形瓶内液面下降,玻璃管中水柱上升,排除了因堵塞而使容器内压强过大引发的爆炸,也使人们立即发现堵塞。
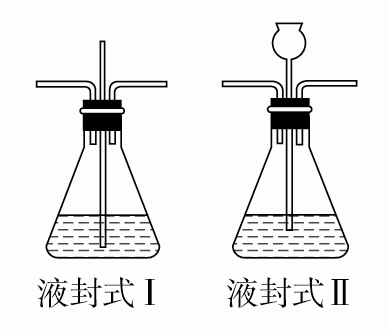
b.恒压式。原理:使分液漏斗与烧瓶内气压相同,保证漏斗中液体顺利流出。
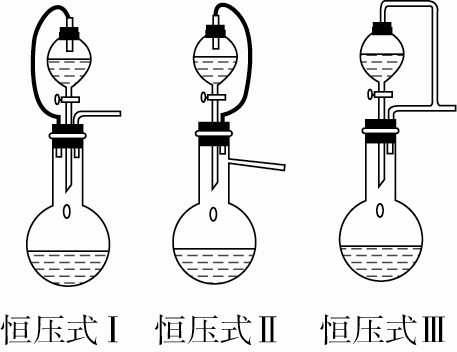
c.防阻式。原理:在较细的导管口处放一团棉花或玻璃丝,防止固体粉末或浆状液体进入导气管而堵塞导管。例如制少量C2H2气体可用防阻式Ⅰ。

⑦防炸裂:普通玻璃制品都有受热不均匀易炸裂的特性,因此a.试管加热时先要预热;b.做固体在气体中燃烧实验时要在集气瓶底预留少量水或铺一层细沙;c.注意防止倒吸;d.热的烧瓶、烧杯、试管等要避免骤冷。
⑧防泄漏:检查装置的气密性、长颈漏斗下端插入液面下以防止气体泄漏;检查滴定管、分液漏斗、容量瓶是否漏水以防止液体泄漏。
⑨防污染:
a.已取出的未用完的试剂一般不放回原瓶(块状固体白磷、钠、钾等除外);
b.用胶头滴管滴加液体时,不伸入瓶内,不接触试管壁(向FeSO4溶液中加NaOH溶液除外);
c.取用试剂时试剂瓶盖倒放于桌面上;
d.药匙和胶头滴管尽可能专用(或洗净、擦干后再取其他药品); e.废液及时处理。
⑩防意外:应设有良好的通风设备,使空气畅通。使用、制备有毒气体和有烟雾的实验应在密闭系统或通风橱中进行,外加尾气吸收处理装置;不可尝药品的味道;误食重金属盐应立即服用生蛋白或生牛奶。
一方面,应遵守实验规则,规范操作,防止各种意外事故发生;另一方面,应熟悉实验室常见事故的处理方法,冷静、果断、正确地处理。