- 从实验到化学从实验到化学
- 过滤与蒸发过滤与蒸发
- 粗盐提纯粗盐提纯
- 蒸馏蒸馏
- 萃取和分液萃取和分液
- 物质的分离与提纯问题1——仪器和方法选择物质的分离与提纯问题1——仪器和方法选择
- 物质的分离与提纯问题2——实验设计与评价物质的分离与提纯问题2——实验设计与评价
- 化学计量在实验中的使用(I)化学计量在实验中的使用(I)
- 物质的量的概念物质的量的概念
- 摩尔质量摩尔质量
- 物质的量和摩尔质量的应用1——与质量或微粒数的换算物质的量和摩尔质量的应用1——与质量或微粒数的换算
- 物质的量和摩尔质量的应用2——用于化学方程式的计算物质的量和摩尔质量的应用2——用于化学方程式的计算
- 物质的量和摩尔质量的应用3——用于相对分子质量的计算物质的量和摩尔质量的应用3——用于相对分子质量的计算
- 物质的量和摩尔质量的应用4——用于混合物计算物质的量和摩尔质量的应用4——用于混合物计算
- 气体摩尔体积的概念气体摩尔体积的概念
- 气体摩尔体积的应用1——用于化学方程式的计算气体摩尔体积的应用1——用于化学方程式的计算
- 气体摩尔体积的应用2——与物质的量、质量、微粒数的换算气体摩尔体积的应用2——与物质的量、质量、微粒数的换算
- 混合物的平均摩尔质量混合物的平均摩尔质量
- 混合气体平均摩尔质量的计算混合气体平均摩尔质量的计算
- 阿伏加德罗定律及其推论阿伏加德罗定律及其推论
- 阿伏伽德罗定律及其推论的应用阿伏伽德罗定律及其推论的应用
- 与物质的量相关的计算1——混合气体的计算与物质的量相关的计算1——混合气体的计算
- 与物质的量相关的计算2——交叉法的使用与物质的量相关的计算2——交叉法的使用
- 化学计量在实验中的使用(II)化学计量在实验中的使用(II)
- 物质的量浓度的概念物质的量浓度的概念
- 溶液中溶质微粒之间的关系溶液中溶质微粒之间的关系
- 物质的量浓度在计算中的应用物质的量浓度在计算中的应用
- 一定物质的量浓度的溶液配制一定物质的量浓度的溶液配制
- 一定物质的量浓度溶液配制的误差分析一定物质的量浓度溶液配制的误差分析
- 溶质的质量分数、物质的量浓度之间换算溶质的质量分数、物质的量浓度之间换算
- 关于溶液稀释或混合的计算关于溶液稀释或混合的计算
- 化学物质及其变化化学物质及其变化
- 物质的分类物质的分类
- 几种分散系几种分散系
- 电解质和电离电解质和电离
- 强电解质和弱电解质强电解质和弱电解质
- 离子反应离子反应
- 离子方程式的概念和书写离子方程式的概念和书写
- 离子反应的发生条件离子反应的发生条件
- 氧化还原反应氧化还原反应
- 氧化还原反应的相关概念氧化还原反应的相关概念
- 氧化剂和还原剂的判断氧化剂和还原剂的判断
- 氧化还原反应中电子转移的表示方法氧化还原反应中电子转移的表示方法
- 归中反应和歧化反应归中反应和歧化反应
- 氧化性与还原性的强弱判断氧化性与还原性的强弱判断
- 氧化还原反应方程式配平的一般方法氧化还原反应方程式配平的一般方法
- 氧化还原反应方程式配平的特殊方法氧化还原反应方程式配平的特殊方法
- 氧化还原反应的应用氧化还原反应的应用
- 金属及其化合物(I)金属及其化合物(I)
- 钠钠
- 钠与铝的氧化物钠与铝的氧化物
- 钠和水的反应钠和水的反应
- 铝的两性铝的两性
- 铝与氢氧化钠溶液的反应原理铝与氢氧化钠溶液的反应原理
- 铁和水蒸气的反应铁和水蒸气的反应
- 金属及其化合物(II)金属及其化合物(II)
- 过氧化钠与水的反应过氧化钠与水的反应
- 过氧化钠的漂白性及其与二氧化碳的反应过氧化钠的漂白性及其与二氧化碳的反应
- 氧化钠和过氧化钠的比较氧化钠和过氧化钠的比较
- 碳酸钠和碳酸氢钠的区别和联系碳酸钠和碳酸氢钠的区别和联系
- 碳酸钠和碳酸氢钠的鉴别碳酸钠和碳酸氢钠的鉴别
- 从矿石中分离提纯铝的简单问题从矿石中分离提纯铝的简单问题
- 从矿石中分离提纯铝的复杂问题从矿石中分离提纯铝的复杂问题
- 铁及其常见化合物铁及其常见化合物
- 氢氧化亚铁的制备氢氧化亚铁的制备
- 铁离子和亚铁离子的鉴别及铁三角铁离子和亚铁离子的鉴别及铁三角
- 金属及其化合物复习1—钠及其化合物金属及其化合物复习1—钠及其化合物
- 金属及其化合物复习2—铝及其化合物金属及其化合物复习2—铝及其化合物
- 金属及其化合物复习3—铁及其化合物金属及其化合物复习3—铁及其化合物
- 金属及其化合物复习4—金属流程综合问题金属及其化合物复习4—金属流程综合问题
- 非金属及其化合物(I)非金属及其化合物(I)
- 硅和二氧化硅硅和二氧化硅
- 硅酸和硅酸盐硅酸和硅酸盐
- 氯气的制备氯气的制备
- 氯气与金属和非金属单质的反应氯气与金属和非金属单质的反应
- 氯水性质的探究氯水性质的探究
- 氯气在生活中的应用氯气在生活中的应用
- 硫与硫化氢硫与硫化氢
- 二氧化硫的性质和制取二氧化硫的性质和制取
- 二氧化硫的漂白性及其应用二氧化硫的漂白性及其应用
- 酸雨的成因和防治酸雨的成因和防治
- 一氧化氮和二氧化氮一氧化氮和二氧化氮
- 氮氧化物的实验室制法氮氧化物的实验室制法
- 一氧化氮和二氧化氮混合溶于水的问题一氧化氮和二氧化氮混合溶于水的问题
- 一氧化氮或二氧化氮与氧气混合溶于水的问题一氧化氮或二氧化氮与氧气混合溶于水的问题
- 非金属及其化合物(II)非金属及其化合物(II)
- 氨气和氨水氨气和氨水
- 氨气的碱性及铵盐的热不稳定性氨气的碱性及铵盐的热不稳定性
- 氨气的还原性氨气的还原性
- 氨气的制备和铵根离子的检验氨气的制备和铵根离子的检验
- 硝酸的性质和工业制法硝酸的性质和工业制法
- 硝酸的强氧化性硝酸的强氧化性
- 稀硫酸的酸性和浓硫酸的吸水性稀硫酸的酸性和浓硫酸的吸水性
- 浓硫酸的脱水性和强氧化性浓硫酸的脱水性和强氧化性
- 硅、氯及其化合物复习硅、氯及其化合物复习
- 氯及其化合物综合实验题氯及其化合物综合实验题
- 硫及其化合物复习硫及其化合物复习
- 二氧化硫的综合实验题二氧化硫的综合实验题
- 氮及其化合物复习氮及其化合物复习
- 氮及其化合物综合实验题氮及其化合物综合实验题
- 浓硫酸的综合实验题浓硫酸的综合实验题
- 物质结构 元素周期律(I)物质结构 元素周期律(I)
- 原子组成与原子符号原子组成与原子符号
- 元素、核素与同位素元素、核素与同位素
- 相对原子质量和核外电子排布规则相对原子质量和核外电子排布规则
- 原子结构的综合应用原子结构的综合应用
- 元素周期表的结构元素周期表的结构
- 原子结构与元素周期表的关系原子结构与元素周期表的关系
- 元素周期律元素周期律
- 同周期元素金属性和非金属性的递变同周期元素金属性和非金属性的递变
- 同主族元素金属性和非金属性的递变同主族元素金属性和非金属性的递变
- 同周期同主族元素性质递变规律总结同周期同主族元素性质递变规律总结
- 元素的金属性或非金属性强弱的判断依据元素的金属性或非金属性强弱的判断依据
- 元素周期表的应用元素周期表的应用
- 10电子微粒和18电子微粒10电子微粒和18电子微粒
- 微粒半径大小比较微粒半径大小比较
- 元素周期律的综合应用1——短周期元素元素周期律的综合应用1——短周期元素
- 元素周期律的综合应用2——陌生元素元素周期律的综合应用2——陌生元素
- 物质结构 元素周期律(II)物质结构 元素周期律(II)
- 离子键离子键
- 共价键共价键
- 电子式的概念电子式的概念
- 复杂的电子式复杂的电子式
- 共价化合物的电子式和结构式共价化合物的电子式和结构式
- 用电子式表示物质的形成用电子式表示物质的形成
- 离子化合物和共价化合物的比较离子化合物和共价化合物的比较
- 分子间作用力分子间作用力
- 氢键氢键
- 化学键的类型和物质的电子式化学键的类型和物质的电子式
- 离子键和共价键的概念辨析离子键和共价键的概念辨析
- 化学键和范德华力与物质形成的关系化学键和范德华力与物质形成的关系
- 与化学键有关的信息给予题与化学键有关的信息给予题
- 化学反应与能量化学反应与能量
- 化学键与反应中的能量关系化学键与反应中的能量关系
- 化学能与热能的相互转化化学能与热能的相互转化
- 从化学键推导化学反应的热效应从化学键推导化学反应的热效应
- 与化学反应热效应相关的探究性实验题与化学反应热效应相关的探究性实验题
- 原电池的工作原理原电池的工作原理
- 原电池的形成条件原电池的形成条件
- 如何设计原电池如何设计原电池
- 发展中的化学电源发展中的化学电源
- 根据原电池的原理分析金属活动性根据原电池的原理分析金属活动性
- 根据氧化还原反应的原理书写原电池的电极反应根据氧化还原反应的原理书写原电池的电极反应
- 化学反应速率化学反应速率
- 化学反应速率的影响因素化学反应速率的影响因素
- 化学反应限度化学反应限度
- 化学平衡状态的判断化学平衡状态的判断
- 有关反应限度的计算方法有关反应限度的计算方法
- 化学反应速率的比较化学反应速率的比较
- 化学平衡状态的判断方法化学平衡状态的判断方法
- 多个条件比较反应速率的问题及转化率的计算多个条件比较反应速率的问题及转化率的计算
- 有机化合物(I)有机化合物(I)
- 甲烷的存在与结构甲烷的存在与结构
- 甲烷的化学性质甲烷的化学性质
- 烷烃的结构特点与性质烷烃的结构特点与性质
- 同系物同系物
- 同分异构体同分异构体
- 烷烃的命名烷烃的命名
- 确定有机物分子式的一般方法确定有机物分子式的一般方法
- 综合计算综合计算
- 乙烯的来源和结构乙烯的来源和结构
- 乙烯的氧化反应乙烯的氧化反应
- 乙烯的加成反应乙烯的加成反应
- 乙烯的综合应用乙烯的综合应用
- 苯的结构和物理性质苯的结构和物理性质
- 苯的化学性质苯的化学性质
- 苯的综合应用苯的综合应用
- 有机化合物(II)有机化合物(II)
- 乙醇的结构和物理性质乙醇的结构和物理性质
- 乙醇的置换反应乙醇的置换反应
- 乙醇的氧化反应乙醇的氧化反应
- 乙醇的综合应用乙醇的综合应用
- 乙酸的结构和性质乙酸的结构和性质
- 乙酸乙酯的制备乙酸乙酯的制备
- 乙酸的综合应用乙酸的综合应用
- 糖类和单糖糖类和单糖
- 双糖和多糖双糖和多糖
- 油脂油脂
- 氨基酸氨基酸
- 蛋白质蛋白质
- 化学与自然资源的开发利用化学与自然资源的开发利用
- 金属冶炼的一般方法金属冶炼的一般方法
- 金属冶炼的特殊方法金属冶炼的特殊方法
- 海水中水资源的利用海水中水资源的利用
- 海水中金属元素的提取海水中金属元素的提取
- 海水中非金属元素的提取海水中非金属元素的提取
- 煤和天然气的综合利用煤和天然气的综合利用
- 石油的综合利用石油的综合利用
- 环境保护与绿色化学环境保护与绿色化学
- 化学反应与能量(I)化学反应与能量(I)
- 反应热与化学键的关系反应热与化学键的关系
- 反应热和物质能量的关系反应热和物质能量的关系
- 常见的放热反应和吸热反应常见的放热反应和吸热反应
- 焓变 反应热 习题课1——根据键能求反应热焓变 反应热 习题课1——根据键能求反应热
- 焓变 反应热 习题课2——根据反应热求键能焓变 反应热 习题课2——根据反应热求键能
- 热化学方程式的概念和书写步骤热化学方程式的概念和书写步骤
- 热化学方程式的正误判断热化学方程式的正误判断
- 根据所给信息书写热化学方程式根据所给信息书写热化学方程式
- 中和热概念中和热概念
- 中和热的测定中和热的测定
- 中和热的实验测定注意事项中和热的实验测定注意事项
- 燃烧热燃烧热
- 反应热、中和热、燃烧热对比反应热、中和热、燃烧热对比
- 能源能源
- 化学反应与能量(II)化学反应与能量(II)
- 盖斯定律内容与证明盖斯定律内容与证明
- 盖斯定律的应用1——计算反应热盖斯定律的应用1——计算反应热
- 盖斯定律的应用2——计算键能盖斯定律的应用2——计算键能
- 盖斯定律的应用3——判断反应热的大小盖斯定律的应用3——判断反应热的大小
- 热化学方程式的书写及正误判断热化学方程式的书写及正误判断
- 根据反应物的性质或盖斯定律比较△H的大小根据反应物的性质或盖斯定律比较△H的大小
- 根据反应进行的程度或反应规律比较△H的大小根据反应进行的程度或反应规律比较△H的大小
- 化学反应速率和化学平衡(I)化学反应速率和化学平衡(I)
- 化学反应速率的概念和计算方法化学反应速率的概念和计算方法
- 化学反应速率的比较方法化学反应速率的比较方法
- 化学反应速率的测量方法化学反应速率的测量方法
- 化学反应速率的微观解释化学反应速率的微观解释
- 影响化学反应速率的因素1—浓度和温度影响化学反应速率的因素1—浓度和温度
- 影响化学反应速率的因素2—压强影响化学反应速率的因素2—压强
- 影响化学反应速率的因素3—催化剂影响化学反应速率的因素3—催化剂
- 总结外界条件对反应速率的影响及本质总结外界条件对反应速率的影响及本质
- 控制变量在速率影响因素中的应用控制变量在速率影响因素中的应用
- 化学反应速率和化学平衡(II)化学反应速率和化学平衡(II)
- 可逆反应与不可逆反应可逆反应与不可逆反应
- 化学平衡状态的概念和特征化学平衡状态的概念和特征
- 等效平衡等效平衡
- 化学平衡状态判断的标志化学平衡状态判断的标志
- 化学平衡常数的概念和计算方法化学平衡常数的概念和计算方法
- 计算化学平衡常数的注意事项计算化学平衡常数的注意事项
- 平衡常数的应用1——计算平衡状态的组成平衡常数的应用1——计算平衡状态的组成
- 平衡常数的应用2——判断反应进行方向平衡常数的应用2——判断反应进行方向
- 影响化学平衡的条件1—浓度影响化学平衡的条件1—浓度
- 影响化学平衡的条件2—压强(1)影响化学平衡的条件2—压强(1)
- 影响化学平衡的条件2—压强(2)影响化学平衡的条件2—压强(2)
- 影响化学平衡的条件3—温度影响化学平衡的条件3—温度
- 影响化学平衡的条件4—催化剂影响化学平衡的条件4—催化剂
- 勒夏特勒原理勒夏特勒原理
- 化学平衡问题解决思路化学平衡问题解决思路
- 勒夏特列原理在工业生产的应用—合成氨条件的选择勒夏特列原理在工业生产的应用—合成氨条件的选择
- 化学平衡中的常见图像1—速率时间曲线图(υ—t图像)化学平衡中的常见图像1—速率时间曲线图(υ—t图像)
- 化学平衡中的常见图像2—含量-时间-温度(压强)图化学平衡中的常见图像2—含量-时间-温度(压强)图
- 化学平衡中的常见图像3—浓度时间图(c—t图像)和恒温(压)线化学平衡中的常见图像3—浓度时间图(c—t图像)和恒温(压)线
- 化学反应速率和化学平衡(III)化学反应速率和化学平衡(III)
- 化学平衡中的常见图像4—其他类型(练习1)化学平衡中的常见图像4—其他类型(练习1)
- 化学平衡中的常见图像4—其他类型(练习2)化学平衡中的常见图像4—其他类型(练习2)
- 化学平衡中的常见图像4—其他类型(练习3)化学平衡中的常见图像4—其他类型(练习3)
- 恒温恒容下不等气反应的等效平衡恒温恒容下不等气反应的等效平衡
- 恒温恒容下等气反应的等效平衡恒温恒容下等气反应的等效平衡
- 恒温恒压下的等效平衡恒温恒压下的等效平衡
- 恒温恒容下不等气反应等效平衡的例题分析恒温恒容下不等气反应等效平衡的例题分析
- 恒温恒容下等气反应等效平衡的例题分析恒温恒容下等气反应等效平衡的例题分析
- 恒温恒压下等效平衡的例题分析恒温恒压下等效平衡的例题分析
- 等效模型等效模型
- 等效模型的实例分析等效模型的实例分析
- 化学平衡的三段式计算化学平衡的三段式计算
- 化学平衡三段式计算的应用化学平衡三段式计算的应用
- 化学平衡移动原理分析实际问题化学平衡移动原理分析实际问题
- 化学反应进行的方向化学反应进行的方向
- 水溶液中的离子平衡(I)水溶液中的离子平衡(I)
- 电解质和非电解质电解质和非电解质
- 强弱电解质对比强弱电解质对比
- 电离方程式的书写电离方程式的书写
- 弱电解质的电离平衡及其影响因素弱电解质的电离平衡及其影响因素
- 弱电解质电离平衡的实例分析弱电解质电离平衡的实例分析
- 一元强酸与一元弱酸的比较一元强酸与一元弱酸的比较
- 电离常数电离常数
- 电离常数的计算电离常数的计算
- 电离平衡与溶液稀释电离平衡与溶液稀释
- 电离平衡与中和反应电离平衡与中和反应
- 水溶液中的离子平衡(II)水溶液中的离子平衡(II)
- 水的电离与水的离子积水的电离与水的离子积
- 水的电离平衡移动水的电离平衡移动
- 溶液的酸碱性溶液的酸碱性
- pHpH
- 由溶液pH推测水的电离情况由溶液pH推测水的电离情况
- 由水的电离情况推测溶液pH由水的电离情况推测溶液pH
- 酸溶液稀释后的pH变化酸溶液稀释后的pH变化
- 碱溶液稀释后的pH变化碱溶液稀释后的pH变化
- 酸溶液的pH和浓度之间的换算酸溶液的pH和浓度之间的换算
- 碱溶液的pH和浓度之间的换算碱溶液的pH和浓度之间的换算
- 强酸与强酸或强碱与强碱混合后的pH计算强酸与强酸或强碱与强碱混合后的pH计算
- 强酸与强碱混合后的pH计算强酸与强碱混合后的pH计算
- 已知强酸和强碱的pH之和,判断等体积混合后溶液的pH已知强酸和强碱的pH之和,判断等体积混合后溶液的pH
- pH的计算的例题分析pH的计算的例题分析
- 酸碱中和滴定酸碱中和滴定
- 酸碱中和滴定操作步骤酸碱中和滴定操作步骤
- 酸碱中和滴定的滴定曲线酸碱中和滴定的滴定曲线
- 中和滴定的误差分析1——洗涤和取液过程中和滴定的误差分析1——洗涤和取液过程
- 中和滴定的误差分析2——滴定和读数过程中和滴定的误差分析2——滴定和读数过程
- 氧化还原滴定氧化还原滴定
- 水溶液中的离子平衡(III)水溶液中的离子平衡(III)
- 盐的水解实质盐的水解实质
- 盐的水解规律盐的水解规律
- 盐的水解特点盐的水解特点
- 多元弱酸盐或弱碱盐的水解多元弱酸盐或弱碱盐的水解
- pH相同的CH3COONa和NaOH水的电离程度比较pH相同的CH3COONa和NaOH水的电离程度比较
- 影响盐类水解的主要因素影响盐类水解的主要因素
- 双水解(互促水解)双水解(互促水解)
- 水解平衡移动的应用水解平衡移动的应用
- 利用盐类水解比较溶液的pH大小利用盐类水解比较溶液的pH大小
- 利用盐类水解比较微粒浓度大小1——一元弱酸盐利用盐类水解比较微粒浓度大小1——一元弱酸盐
- 利用盐类水解比较微粒浓度大小2——二元弱酸盐利用盐类水解比较微粒浓度大小2——二元弱酸盐
- 利用盐类水解比较微粒浓度大小3——酸式盐利用盐类水解比较微粒浓度大小3——酸式盐
- 利用盐类水解比较微粒浓度大小4——一元弱酸和盐混合利用盐类水解比较微粒浓度大小4——一元弱酸和盐混合
- 利用盐类水解比较微粒浓度大小5——二元弱酸和酸式盐混合利用盐类水解比较微粒浓度大小5——二元弱酸和酸式盐混合
- 利用盐类水解比较微粒浓度大小的一般方法和步骤利用盐类水解比较微粒浓度大小的一般方法和步骤
- 盐类水解反应的应用1——制备物质盐类水解反应的应用1——制备物质
- 盐类水解反应的应用2——分析离子共存和除杂问题盐类水解反应的应用2——分析离子共存和除杂问题
- 盐类水解反应的应用3——在生活和生产中的应用盐类水解反应的应用3——在生活和生产中的应用
- 水溶液中的离子平衡(IV)水溶液中的离子平衡(IV)
- 沉淀溶解平衡的概念和特征沉淀溶解平衡的概念和特征
- 溶度积常数和溶解平衡移动溶度积常数和溶解平衡移动
- 溶解平衡移动的应用1——沉淀的溶解溶解平衡移动的应用1——沉淀的溶解
- 溶解平衡移动的应用2——沉淀的转化溶解平衡移动的应用2——沉淀的转化
- 溶解平衡移动的应用3——沉淀的转化后除去溶解平衡移动的应用3——沉淀的转化后除去
- 溶度积、溶解度和物质的量浓度之间的换算溶度积、溶解度和物质的量浓度之间的换算
- 自然界和生活中的沉淀溶解平衡自然界和生活中的沉淀溶解平衡
- 电化学基础(I)电化学基础(I)
- 原电池的工作原理原电池的工作原理
- 双液电池工作原理双液电池工作原理
- 原电池原理的应用原电池原理的应用
- 一次电池——锌锰电池一次电池——锌锰电池
- 一次电池——银锌电池和锂电池一次电池——银锌电池和锂电池
- 二次电池——铅蓄电池二次电池——铅蓄电池
- 二次电池——锂离子电池二次电池——锂离子电池
- 化学电源—氢氧燃料电池化学电源—氢氧燃料电池
- 化学电源—甲烷燃料电池化学电源—甲烷燃料电池
- 化学电源—甲醇燃料电池化学电源—甲醇燃料电池
- 化学电源—熔融盐电池化学电源—熔融盐电池
- 电化学基础(II)电化学基础(II)
- 电解原理电解原理
- 电解反应类型1——水或溶质参与反应电解反应类型1——水或溶质参与反应
- 电解反应类型2——离子或电极材料参与反应电解反应类型2——离子或电极材料参与反应
- 电解反应实例分析1——只有水参与反应电解反应实例分析1——只有水参与反应
- 电解反应实例分析2——只有电解质参与反应电解反应实例分析2——只有电解质参与反应
- 电解反应实例分析3——电解质和水都参与反应电解反应实例分析3——电解质和水都参与反应
- 电解原理的应用1——氯碱工业电解原理的应用1——氯碱工业
- 电解原理的应用2——电镀和电冶金电解原理的应用2——电镀和电冶金
- 电解原理的应用3——精炼铜电解原理的应用3——精炼铜
- 原电池和电解池的区别和联系原电池和电解池的区别和联系
- 再看可逆电池再看可逆电池
- 有关电化学的计算1——两极产物或pH的计算有关电化学的计算1——两极产物或pH的计算
- 有关电化学的计算2——相对原子质量的计算有关电化学的计算2——相对原子质量的计算
- 有关电化学的计算3——转移电子的量和产物的量有关电化学的计算3——转移电子的量和产物的量
- 氯碱工业原理的应用氯碱工业原理的应用
- 电解电解质溶液的分析方法与规律电解电解质溶液的分析方法与规律
- 金属的电化学腐蚀金属的电化学腐蚀
- 析氢腐蚀和吸氧腐蚀的比较析氢腐蚀和吸氧腐蚀的比较
- 金属的电化学防护金属的电化学防护
- 认识有机化合物认识有机化合物
- 烃及其分类烃及其分类
- 烃的衍生物及其分类烃的衍生物及其分类
- 有机物的常见原子的成键特点有机物的常见原子的成键特点
- 有机物的空间结构有机物的空间结构
- 同分异构体同分异构体
- 烯烃炔烃的命名烯烃炔烃的命名
- 苯的同系物的命名苯的同系物的命名
- 有机物的分离和提纯1-蒸馏有机物的分离和提纯1-蒸馏
- 有机物的分离和提纯2-重结晶有机物的分离和提纯2-重结晶
- 有机物的分离和提纯3-萃取与分液有机物的分离和提纯3-萃取与分液
- 有机物最简式(实验式)的确定有机物最简式(实验式)的确定
- 相对分子质量的确定—质谱法相对分子质量的确定—质谱法
- 分子结构的鉴定—红外光谱分子结构的鉴定—红外光谱
- 分子结构的鉴定—核磁共振氢谱分子结构的鉴定—核磁共振氢谱
- 研究有机物的一般步骤和方法研究有机物的一般步骤和方法
- 烃和卤代烃(I)烃和卤代烃(I)
- 脂肪烃1-烷烃脂肪烃1-烷烃
- 脂肪烃2-烯烃的组成和同分异构脂肪烃2-烯烃的组成和同分异构
- 脂肪烃3-烯烃的性质脂肪烃3-烯烃的性质
- 脂肪烃4-烯烃的加聚反应脂肪烃4-烯烃的加聚反应
- 乙烯的实验室制备乙烯的实验室制备
- 乙炔的结构和性质乙炔的结构和性质
- 乙炔的实验室制法乙炔的实验室制法
- 炔烃的结构与性质炔烃的结构与性质
- 乙烷、乙烯、乙炔的对比乙烷、乙烯、乙炔的对比
- 苯的结构和物理性质苯的结构和物理性质
- 苯的取代反应苯的取代反应
- 苯的氧化反应和加成反应苯的氧化反应和加成反应
- 苯的同系物的组成、结构和同分异构苯的同系物的组成、结构和同分异构
- 苯的同系物的性质苯的同系物的性质
- 烃和卤代烃(II)烃和卤代烃(II)
- 溴乙烷的结构和取代反应溴乙烷的结构和取代反应
- 溴乙烷的消去反应溴乙烷的消去反应
- 检验溴乙烷消去反应中的溴离子检验溴乙烷消去反应中的溴离子
- 卤代烃卤代烃
- 卤代烃的综合应用卤代烃的综合应用
- 烃复习1-烃的分类、同系物烃复习1-烃的分类、同系物
- 烃复习2-同分异构体的书写方法1烃复习2-同分异构体的书写方法1
- 烃复习2-同分异构体的书写方法2烃复习2-同分异构体的书写方法2
- 烃复习3-分子的空间结构问题烃复习3-分子的空间结构问题
- 烃复习4-烃和烃的含氧衍生物的燃烧规律1烃复习4-烃和烃的含氧衍生物的燃烧规律1
- 烃复习4-烃和烃的含氧衍生物的燃烧规律2烃复习4-烃和烃的含氧衍生物的燃烧规律2
- 烃复习5-实验-物质的分离与提纯烃复习5-实验-物质的分离与提纯
- 烃复习6-实验-物质的制备烃复习6-实验-物质的制备
- 烃的含氧衍生物(I)烃的含氧衍生物(I)
- 醇的结构特征和命名醇的结构特征和命名
- 醇类的同分异构体醇类的同分异构体
- 重要醇的物理性质及简单应用重要醇的物理性质及简单应用
- 醇类的化学性质1——置换反应和取代反应醇类的化学性质1——置换反应和取代反应
- 醇类的化学性质2——燃烧和催化氧化醇类的化学性质2——燃烧和催化氧化
- 醇类的化学性质3——与强氧化剂的反应醇类的化学性质3——与强氧化剂的反应
- 醇类的化学性质4——消去反应醇类的化学性质4——消去反应
- 醇类的化学性质5——结构与性质的关系醇类的化学性质5——结构与性质的关系
- 苯酚1——苯酚及其同系物苯酚1——苯酚及其同系物
- 苯酚2——物理性质和酸性苯酚2——物理性质和酸性
- 苯酚3——苯酚的弱酸性苯酚3——苯酚的弱酸性
- 苯酚4——取代反应和显色反应苯酚4——取代反应和显色反应
- 苯酚5——加成反应和缩聚反应苯酚5——加成反应和缩聚反应
- 证明羟基和苯环的相互影响证明羟基和苯环的相互影响
- 分离苯和苯酚分离苯和苯酚
- 处理含有苯酚的废水处理含有苯酚的废水
- 烃的含氧衍生物(II)烃的含氧衍生物(II)
- 醛的结构特征和同分异构体醛的结构特征和同分异构体
- 乙醛的性质1——加成反应和氧化反应乙醛的性质1——加成反应和氧化反应
- 乙醛的性质2——银镜反应乙醛的性质2——银镜反应
- 乙醛的性质3——与新制氢氧化铜反应乙醛的性质3——与新制氢氧化铜反应
- 甲醛的性质甲醛的性质
- 醛类的化学性质醛类的化学性质
- 羧酸的结构特征羧酸的结构特征
- 常见羧酸的物理性质和羧酸的通性常见羧酸的物理性质和羧酸的通性
- 羧酸的酯化反应羧酸的酯化反应
- 验证乙酸、碳酸和苯酚的酸性强弱验证乙酸、碳酸和苯酚的酸性强弱
- 酯的结构特征和性质酯的结构特征和性质
- 酯类的异构酯类的异构
- 各类酯化反应各类酯化反应
- 各类酯的水解反应各类酯的水解反应
- 烃的含氧衍生物(III)烃的含氧衍生物(III)
- 各类有机物的转化关系各类有机物的转化关系
- 烃的衍生物的主要类别及主要化学性质烃的衍生物的主要类别及主要化学性质
- 有机反应类型1——取代反应有机反应类型1——取代反应
- 有机反应类型2——加成反应有机反应类型2——加成反应
- 有机反应类型3——消去反应和还原反应有机反应类型3——消去反应和还原反应
- 有机反应类型4——加聚反应有机反应类型4——加聚反应
- 有机反应类型5——缩聚反应有机反应类型5——缩聚反应
- 有机反应类型6——氧化反应有机反应类型6——氧化反应
- 有机合成的过程1——官能团的转化有机合成的过程1——官能团的转化
- 有机合成的过程2——卤代烃的应用有机合成的过程2——卤代烃的应用
- 有机合成的方法1——正向合成分析法有机合成的方法1——正向合成分析法
- 有机合成的方法2——逆向合成分析法有机合成的方法2——逆向合成分析法
- 生命中的基础有机化学物质生命中的基础有机化学物质
- 油脂的结构特征和物理性质油脂的结构特征和物理性质
- 油脂的化学性质油脂的化学性质
- 肥皂的去污原理和合成洗涤剂肥皂的去污原理和合成洗涤剂
- 糖类定义和分类糖类定义和分类
- 葡萄糖和果糖葡萄糖和果糖
- 蔗糖和麦芽糖蔗糖和麦芽糖
- 淀粉和纤维素淀粉和纤维素
- 进入合成有机高分子化合物的时代进入合成有机高分子化合物的时代
- 有机化学知识归纳与整理有机化学知识归纳与整理
《铝与氢氧化钠溶液的反应原理》铝与氢氧化钠溶液的反应原理
1单选题
如图所示的实验中,投入铝片后 ( )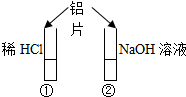
题目答案
您的答案
答案解析
分析:
Al既能与盐酸反应生成氢气,又能与氢氧化钠溶液反应生成氢气,反应分别为2Al+6HCl=2AlCl$_3$+3H$_2$↑、2Al+2NaOH+2H$_2$O=2NaAlO$_2$ +3H$_2$↑.
解答:
解:A、因②中发生2Al+2NaOH+2H$_2$O=2NaAlO$_2$ +3H$_2$↑,则②中产生气泡,故A错误;
B、因①中发生2Al+6HCl=2AlCl$_3$+3H$_2$↑,②中发生2Al+2NaOH+2H$_2$O=2NaAlO$_2$ +3H$_2$↑,则①和②中都产生气泡,故B错误;
C、因①中发生2Al+6HCl=2AlCl$_3$+3H$_2$↑,②中发生2Al+2NaOH+2H$_2$O=2NaAlO$_2$ +3H$_2$↑,则都有气泡,且生成的都是H$_2$,故C错误;
D、因①中发生2Al+6HCl=2AlCl$_3$+3H$_2$↑,②中发生2Al+2NaOH+2H$_2$O=2NaAlO$_2$ +3H$_2$↑,则都有气泡,且生成的都是H$_2$,故D正确;
故选D.
点评:
本题考查Al的化学性质,明确Al与酸、碱的化学反应是解答本题的关键,难度不大,注重对基础知识的考查.
2单选题
铝制器皿能够盛放的物质是( )
题目答案
您的答案
答案解析
分析:
能持续发生反应则不能用铝制容器来盛放,铝能与强酸、强碱反应,能与一些盐反应等,在浓硫酸、浓硝酸中发生钝化,据此结合选项判断即可.
解答:
解:A、铝与氢氧化钾溶液反应生成偏铝酸钾与氢气,不能用铝制品容器盛放,故A错误;
B、浓硫酸是强氧化性的酸,铝在浓硫酸中发生钝化现象,故铝制品容器可以盛放浓硫酸,故B正确;
C、铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,不能用铝制品容器盛放,故C错误;
D、稀硫酸有弱氧化性,能和铝反应生成氢气,不能用铝制品容器盛放,故D错误;
故选B.
点评:
本题考查了铝的化学性质,比较基础,注意铁、铝都能和浓硫酸、浓硝酸在常温下发生钝化现象.
3单选题
在两个烧杯中分别盛有100mL 3.0mol•L_的盐酸和氢氧化钠溶液,向两个烧杯中分别加入等质量的铝粉,在相同状况下生成的气体的体积比为2:5,则加入的铝粉的质量为( )
题目答案
您的答案
答案解析
分析:
根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,反应结束后测得生成的气体体积比为甲:乙=2:5,由化学反应方程式可知,酸与金属反应时,酸不足量,碱与金属反应时碱过量来计算解答.
解答:
解:盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×3mol/L=0.3mol,
又两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=2:5,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,
则 2Al+6HCl═2AlCl$_3$+3H$_2$↑
6 3
0.3mol x
$\frac {6}{3}$=$\frac {0.3mol}{x}$,解得x=0.15mol,
一定条件下,气体的物质的量之比等于体积之比,
则碱与金属铝反应生成的氢气的物质的量为0.15mol×$\frac {5}{2}$=0.375mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,
则 2Al+2NaOH+2H$_2$O═2NaAlO$_2$+3H$_2$↑
2 3
y 0.375mol
$\frac {2}{x}$=$\frac {3}{0.375}$,解得y=0.25mol,
则铝的质量为0.25mol×27g/mol=6.75g,
故选:B.
点评:
本题考查学生利用化学反应方程式的计算,正确判断酸碱是否过量是解本题关键,再结合反应方程式来分析解答,难度中等.
4单选题
两份铝屑,一份与过量HCl反应,另一份与过量NaOH溶液反应,产生的H$_2$在相同条件下体积比为1:1,则两份铝屑的质量比为( )
题目答案
您的答案
答案解析
分析:
根据铝跟盐酸或氢氧化钠溶液都能发生反应,利用化学方程式的特点即可看出生成相同质量的氢气时金属质量的多少.
解答:
解:观察铝反应得到氢气的方程式:2Al+6HCl=2AlCl$_3$+3H$_2$↑,2Al+2NaOH+2H$_2$O=2NaAlO$_2$+3H$_2$↑,发现了如下的规律.当都生成相同的氢气时消耗的铝的质量应该相等,也就是质量比是1:1.
故选A.
点评:
本题主要考查学生对参加反应的物质质量的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.
5单选题
常温下,下列溶液可以用铝槽车装运的是( )
题目答案
您的答案
答案解析
分析:
铝能与盐酸、稀硫酸、氢氧化钠溶液、稀硝酸反应,但常温下铝在浓硫酸、浓硝酸中发生钝化,可以用铝槽车装运,据此判断.
解答:
解:A.铝和氢氧化钠溶液反应,生成NaAlO$_2$、H$_2$,反应为:2Al+2NaOH+2H$_2$O=2NaAlO$_2$+3H$_2$↑,所以不能用铝槽车来运送,故A错误;
B.铝与浓盐酸反应2Al+6HCl=2AlCl$_3$+3H$_2$↑,生成氯化铝和氢气,故不能用铝槽车来运送,故B错误;
C.常温下,铝在浓硝酸中发生钝化现象,生成一层致密的氧化物保护膜,阻止内部金属与浓硝酸继续反应,故能用铝槽车来运送,故C正确;
D.铝在稀硝酸中不能发生钝化,铝与稀硝酸反应Al+4HNO$_3$(稀)=Al(NO$_3$)$_3$+NO↑+2H$_2$O,故不能用铝槽车来运送,故D错误;
故选C.
点评:
本题考查铝的性质,难度较小,注意钝化现象为常温,常见金属为铁、铝在浓硫酸、浓硝酸发生钝化.
6单选题
[2010·湖南期末]把一块Al、Fe合金放入足量盐酸中,通入足量的Cl$_2$,再加过量NaOH溶液、过滤,把滤渣充分灼烧,得到固体残留物恰好与原合金质量相等,则合金中Fe、Al质量比为( )
题目答案
您的答案
答案解析
分析:
解答:
点评:
本题考查根据方程式计算及物质性质、铝及化合物的性质,难度中等,关键清楚反应过程,本题若用常见解法比较繁琐,本解法关键在于判断合金中Fe、Al质量比为氧化铁中铁元素与氧元素质量之比.
7单选题
取两份等质量的铝分别溶于足量硫酸、足量氢氧化钠溶液中,完全反应后收集到(标准状况下)氢气体积比为( )
题目答案
您的答案
答案解析
分析:
发生反应:2Al+3H$_2$SO$_4$=Al$_2$(SO$_4$)$_3$+3H$_2$↑、2Al+2NaOH+2H$_2$O=2NaAlO$_2$+3H$_2$↑,参加反应Al的质量相等,结合方程式判断.
解答:
解:分别发生反应:2Al+3H$_2$SO$_4$=Al$_2$(SO4)$_3$+3H$_2$↑、2Al+2NaOH+2H$_2$O=2NaAlO$_2$+3H$_2$↑,参加反应Al的质量相等,由方程式可知生成氢气的体积相等,即收集氢气的体积之比为1:1,故选A.
点评:
本题考查化学方程式的有关计算,比较基础,侧重对基础知识的巩固,可以利用电子转移守恒解答.
8单选题
常温下能用铝制容器盛放的是( )
题目答案
您的答案
答案解析
分析:
根据铝的性质进行解答,能持续发生反应则不能用铝制容器来盛放.
解答:
解:A、盐酸是弱氧化性的酸,能和铝反应生成氢气,不能用铝制品容器盛放,故A错误;
B、稀硝酸是强氧化性的酸,能和铝反应,不能用铝制品容器盛放,故B错误;
C、稀硫酸有弱氧化性,能和铝反应生成氢气,不能用铝制品容器盛放,故C错误;
D、铝在浓硝酸中发生钝化现象,故铝制品容器可以盛放浓硝酸,故D正确.
故选D.
点评:
本题考查了铝的化学性质,铁、铝都能和浓硫酸、浓硝酸在常温下发生钝化现象,所以可用铁、铝制容器盛放浓硫酸、浓硝酸.
9单选题
通常情况下,下列物质可用铝制槽车装运的是( )
题目答案
您的答案
答案解析
分析:
铝能与盐酸、稀硫酸、氢氧化钠溶液、稀硝酸反应,但常温下铝在浓硫酸、浓硝酸中发生钝化,可以用铝槽车装运,据此判断.
解答:
解:A.铝与稀盐酸反应2Al+6HCl=2AlCl$_3$+3H$_2$↑,生成氯化铝和氢气,故不能用铝槽车来运送,故A错误;
B.常温下,铝在浓硫酸中发生钝化现象,生成一层致密的氧化物保护膜,阻止内部金属与浓硫酸继续反应,故能用铝槽车来运送,故B正确;
C.铝在稀硝酸中不能发生钝化,铝与稀硝酸反应Al+4HNO$_3$(稀)=Al(NO$_3$)$_3$+NO↑+2H$_2$O,故不能用铝槽车来运送,故C错误;
D.铝和氢氧化钠溶液反应,生成NaAlO$_2$、H$_2$,反应为:2Al+2NaOH+2H$_2$O=2NaAlO$_2$+3H$_2$↑,所以不能用铝槽车来运送,故D错误;
故选B.
点评:
本题考查铝的性质,难度较小,注意钝化现象为常温,常见金属为铁、铝在浓硫酸、浓硝酸发生钝化.
10单选题
下列溶液可用铝槽或铁罐盛放的是( )
题目答案
您的答案
答案解析
分析:
铝性质活泼,可与强碱或强酸溶液反应,与浓硫酸或浓硝酸发生钝化反应,以此解答该题.
解答:
解:铝性质活泼,可与强碱或强酸溶液反应,则题中盐酸、稀盐酸或稀硝酸不能用铝槽或铁罐盛放,
但与浓硫酸或浓硝酸发生钝化反应,在表面生成一层致密的氧化物膜,阻碍反应的继续进行,则可用与盛放浓硫酸.
故选C.
点评:
本题考查铝的性质,为元素化合物中重要知识,本题侧重于基础知识的考查,难度不大,注意铝与浓硫酸、浓硝酸发生钝化的性质.