- 运动的描述(I)运动的描述(I)
- 运动与质点运动与质点
- 参考系参考系
- 坐标系坐标系
- 时间时间
- 时间的计量时间的计量
- 长度的计量长度的计量
- 位移位移
- 矢量和标量矢量和标量
- 一维及二维平面求解路程、位移一维及二维平面求解路程、位移
- 三维空间求解路程、位移三维空间求解路程、位移
- 运动的描述(II)运动的描述(II)
- 速度速度
- 平均速度和瞬时速度平均速度和瞬时速度
- 速度和速率的区别速度和速率的区别
- 从直线运动的x-t图象看速度从直线运动的x-t图象看速度
- 打点计时器打点计时器
- 打点计时器使用步骤与纸带处理打点计时器使用步骤与纸带处理
- 频闪照相和数据处理频闪照相和数据处理
- 光电计时系统光电计时系统
- 超声波测速超声波测速
- 加速度加速度
- 加速度、速度的变化量、速度的关系加速度、速度的变化量、速度的关系
- 从速度时间图象看加速度从速度时间图象看加速度
- 三种运动图象的比较三种运动图象的比较
- 匀变速直线运动的研究(I)匀变速直线运动的研究(I)
- 利用打点计时器研究物体速度的变化利用打点计时器研究物体速度的变化
- 利用纸带画出v-t图象利用纸带画出v-t图象
- 利用纸带求物体加速度的两种方法利用纸带求物体加速度的两种方法
- 各种直线运动的v-t图象各种直线运动的v-t图象
- v-t图象的面积含义v-t图象的面积含义
- v-t图象面积的进一步讨论v-t图象面积的进一步讨论
- 速度与时间的关系速度与时间的关系
- 中点时刻速度与平均速度中点时刻速度与平均速度
- 利用贴纸条法画出v-t图象利用贴纸条法画出v-t图象
- 位移与时间关系位移与时间关系
- 匀变速直线运动连续相等时间位移特点匀变速直线运动连续相等时间位移特点
- 利用打点计时器研究匀变速直线运动物体的加速度利用打点计时器研究匀变速直线运动物体的加速度
- 速度与位移关系速度与位移关系
- 匀变速直线运动中点位移的速度公式匀变速直线运动中点位移的速度公式
- 初速为零的匀变速直线运动特点(1)初速为零的匀变速直线运动特点(1)
- 初速度为零匀变速直线运动特点(2)初速度为零匀变速直线运动特点(2)
- 将匀减速直线运动看成匀加速直线运动将匀减速直线运动看成匀加速直线运动
- 相遇与追及之追及问题相遇与追及之追及问题
- 相遇与追及之防碰撞问题相遇与追及之防碰撞问题
- 追及与相遇问题的变换参考系解法追及与相遇问题的变换参考系解法
- 追及与相遇问题的图象解法追及与相遇问题的图象解法
- 匀变速直线运动的研究(II)匀变速直线运动的研究(II)
- 自由落体运动自由落体运动
- 应用自由落体运动规律解题应用自由落体运动规律解题
- 自由落体运动规律的灵活运用自由落体运动规律的灵活运用
- 测重力加速度测重力加速度
- 自由落体运动规律的实际应用自由落体运动规律的实际应用
- 自由落体运动的综合问题自由落体运动的综合问题
- 竖直上抛运动竖直上抛运动
- 应用竖直上抛运动规律解题应用竖直上抛运动规律解题
- 竖直上抛运动中的相遇问题(1)竖直上抛运动中的相遇问题(1)
- 竖直上抛运动中的相遇问题(2)竖直上抛运动中的相遇问题(2)
- 伽利略的逻辑猜想与实验伽利略的逻辑猜想与实验
- 相互作用力(I)相互作用力(I)
- 力的特性(1)力的特性(1)
- 力的特性(2)力的特性(2)
- 重力重力
- 重力的方向重力的方向
- 重心重心
- 复杂物体的重心复杂物体的重心
- 形变与弹性形变形变与弹性形变
- 几种常见的弹力几种常见的弹力
- 弹力的方向弹力的方向
- 弹力有无的判断弹力有无的判断
- 弹力大小与胡克定律弹力大小与胡克定律
- 胡克定律的理解与应用胡克定律的理解与应用
- 弹簧测力计的使用及读数弹簧测力计的使用及读数
- 弹簧的串联弹簧的串联
- 弹簧的并联弹簧的并联
- 相互作用力(II)相互作用力(II)
- 摩擦力产生的条件摩擦力产生的条件
- 静摩擦力静摩擦力
- 滑动摩擦力滑动摩擦力
- 摩擦因数的测量摩擦因数的测量
- 摩擦力方向的判断方法摩擦力方向的判断方法
- 传送带摩擦力方向的判断方法传送带摩擦力方向的判断方法
- 摩擦力大小的计算摩擦力大小的计算
- 摩擦力的深入理解摩擦力的深入理解
- 矢量运算法则矢量运算法则
- 合力与分力的概念合力与分力的概念
- 探究共点力的合成法则的实验操作探究共点力的合成法则的实验操作
- 探究共点力的合成法则的实验误差分析探究共点力的合成法则的实验误差分析
- 力的平行四边形定则力的平行四边形定则
- 合力与分力的大小和方向关系合力与分力的大小和方向关系
- 在一定条件下进行力的分解在一定条件下进行力的分解
- 按照力的作用效果进行力的分解按照力的作用效果进行力的分解
- 力的正交分解力的正交分解
- 相互作用力(III)相互作用力(III)
- 正交分解法处理平衡问题正交分解法处理平衡问题
- 摩擦力相关的平衡问题(1)摩擦力相关的平衡问题(1)
- 摩擦力相关的平衡问题(2)摩擦力相关的平衡问题(2)
- 力的反向法处理三力平衡问题力的反向法处理三力平衡问题
- 三角形法则处理三力平衡问题三角形法则处理三力平衡问题
- 三角形法则处理力的变化问题三角形法则处理力的变化问题
- 整体法处理系统平衡问题整体法处理系统平衡问题
- 整体+隔离的方法研究系统平衡问题整体+隔离的方法研究系统平衡问题
- 牛顿运动定律(I)牛顿运动定律(I)
- 牛顿第一定律牛顿第一定律
- 惯性与质量惯性与质量
- 实验:探究加速度与力、质量的关系实验:探究加速度与力、质量的关系
- 实验:探究加速度与力、质量的关系的数据分析实验:探究加速度与力、质量的关系的数据分析
- 实验:探究加速度与力、质量的关系的误差分析实验:探究加速度与力、质量的关系的误差分析
- 牛顿第二定律牛顿第二定律
- 牛顿第二定律中F代表合外力牛顿第二定律中F代表合外力
- 牛顿第二定律的矢量性与瞬时性牛顿第二定律的矢量性与瞬时性
- 牛顿第二定律的同体性与独立性牛顿第二定律的同体性与独立性
- 牛顿第二定律——突变问题牛顿第二定律——突变问题
- 力学单位制力学单位制
- 力学单位制之量纲分析法力学单位制之量纲分析法
- 牛顿第三定律牛顿第三定律
- 作用力、反作用力与平衡力的比较作用力、反作用力与平衡力的比较
- 牛顿第三定律应用实例牛顿第三定律应用实例
- 粗糙面上拔河问题粗糙面上拔河问题
- 光滑面上拔河问题光滑面上拔河问题
- 用牛顿第三定律进行受力分析用牛顿第三定律进行受力分析
- 牛顿运动定律(II)牛顿运动定律(II)
- 已知力求运动的问题已知力求运动的问题
- 已知运动求力的问题已知运动求力的问题
- 水平传送带问题水平传送带问题
- 斜面传送带问题斜面传送带问题
- 加速度相同的连接体问题加速度相同的连接体问题
- 超重和失重的原理超重和失重的原理
- 超重和失重的应用超重和失重的应用
- 带滑轮的连接体问题带滑轮的连接体问题
- 系统的牛顿第二定律系统的牛顿第二定律
- 板块模型板块模型
- 动力学中的图象问题动力学中的图象问题
- 摩擦力的临界问题摩擦力的临界问题
- 与绳子有关的临界问题与绳子有关的临界问题
- 物体间分离的临界问题物体间分离的临界问题
- 曲线运动(I)曲线运动(I)
- 曲线运动曲线运动
- 物体做曲线运动的条件物体做曲线运动的条件
- 曲线运动中力对速度的改变曲线运动中力对速度的改变
- 运动的合成与分解运动的合成与分解
- 两个直线运动的合运动性质的判断两个直线运动的合运动性质的判断
- 小船如何渡河时间最短?小船如何渡河时间最短?
- 小船如何渡河距离最短?小船如何渡河距离最短?
- 绳子的“关联”速度问题绳子的“关联”速度问题
- 杆以及相互接触物体的“关联”速度问题杆以及相互接触物体的“关联”速度问题
- 变换参考系相关的运动合成与分解变换参考系相关的运动合成与分解
- 曲线运动(II)曲线运动(II)
- 平抛运动特点平抛运动特点
- 平抛运动的位移分析平抛运动的位移分析
- 平抛运动的速度分析平抛运动的速度分析
- 频闪照相下的平抛运动分析频闪照相下的平抛运动分析
- 平抛运动的速度矢量图平抛运动的速度矢量图
- 平抛运动中位移与水平夹角的应用平抛运动中位移与水平夹角的应用
- 平抛运动中速度与水平夹角的应用平抛运动中速度与水平夹角的应用
- 斜抛运动斜抛运动
- 抛铅球的最佳角度抛铅球的最佳角度
- 将斜抛运动到最高点看作平抛运动的逆过程将斜抛运动到最高点看作平抛运动的逆过程
- 研究平抛运动的实验装置和方法研究平抛运动的实验装置和方法
- 求平抛运动的初速度求平抛运动的初速度
- 求平抛运动初速度的其他方法求平抛运动初速度的其他方法
- 曲线运动(III)曲线运动(III)
- 圆周运动的线速度圆周运动的线速度
- 圆周运动的角速度、周期和频率圆周运动的角速度、周期和频率
- 描述圆周运动物理量之间的关系描述圆周运动物理量之间的关系
- 三种传动装置三种传动装置
- 圆周运动与直线运动的综合问题圆周运动与直线运动的综合问题
- 向心加速度的推导向心加速度的推导
- 向心加速度的理解与应用向心加速度的理解与应用
- 向心力向心力
- 向心力的验证向心力的验证
- 水平面的圆周运动水平面的圆周运动
- 圆锥摆的周期圆锥摆的周期
- 临界态匀速圆周运动问题临界态匀速圆周运动问题
- 变速圆周运动的受力变速圆周运动的受力
- 相互连接物体的临界态问题相互连接物体的临界态问题
- 一般的曲线运动一般的曲线运动
- 曲线运动(IV)曲线运动(IV)
- 汽车拐弯问题汽车拐弯问题
- 火车、飞机拐弯问题火车、飞机拐弯问题
- 拱形桥和下凹桥问题拱形桥和下凹桥问题
- 航天器中的失重现象航天器中的失重现象
- 绳子连接小球在竖直面内做变速圆周运动绳子连接小球在竖直面内做变速圆周运动
- 硬杆连接小球在竖直面内做匀速圆周运动硬杆连接小球在竖直面内做匀速圆周运动
- 向心运动与离心运动向心运动与离心运动
- 万有引力与航天(I)万有引力与航天(I)
- 天文学历史简介天文学历史简介
- 开普勒三定律开普勒三定律
- 开普勒三定律的应用开普勒三定律的应用
- 太阳与行星间的引力太阳与行星间的引力
- 月—地检验月—地检验
- 万有引力定律万有引力定律
- 卡文迪许的扭秤实验卡文迪许的扭秤实验
- “黄金代换”公式“黄金代换”公式
- 重力与万有引力的关系重力与万有引力的关系
- 万有引力定律的推论万有引力定律的推论
- 万有引力定律的成就万有引力定律的成就
- 万有引力与航天(II)万有引力与航天(II)
- 行星追及和最大观测角问题行星追及和最大观测角问题
- 行星椭圆轨道运动的时间问题行星椭圆轨道运动的时间问题
- 卫星的可视性问题卫星的可视性问题
- 求星球质量的几种方法求星球质量的几种方法
- 求星球密度的几种方法求星球密度的几种方法
- 利用一块手表测量星球密度利用一块手表测量星球密度
- 人造卫星的轨道人造卫星的轨道
- 同步卫星同步卫星
- 卫星的失重卫星的失重
- 万有引力与航天(III)万有引力与航天(III)
- 牛顿大炮牛顿大炮
- 第一宇宙速度第一宇宙速度
- 第二、第三宇宙速度第二、第三宇宙速度
- 几类卫星的比较几类卫星的比较
- 卫星变轨问题卫星变轨问题
- 人造卫星的多次变轨问题人造卫星的多次变轨问题
- 双星双星
- 黑洞与暗物质黑洞与暗物质
- 低速低速
- 宏观、弱引力宏观、弱引力
- 机械能守恒定律(I)机械能守恒定律(I)
- 能量、动能、势能能量、动能、势能
- 功功
- 正功与负功正功与负功
- 恒力做功恒力做功
- 弹力做功问题弹力做功问题
- 静摩擦力做功问题静摩擦力做功问题
- 滑动摩擦力做功问题滑动摩擦力做功问题
- 变力做功问题变力做功问题
- 作用力与反作用力做功问题作用力与反作用力做功问题
- 机械能守恒定律(II)机械能守恒定律(II)
- 功率功率
- 恒力做功的功率恒力做功的功率
- 机车恒功率启动机车恒功率启动
- 机车匀加速启动机车匀加速启动
- 重力做功与重力势能重力做功与重力势能
- 重力做功与重力势能的关系重力做功与重力势能的关系
- 与重心变化有关的重力做功与重心变化有关的重力做功
- 弹性势能的概念和表达式弹性势能的概念和表达式
- 弹性势能的计算弹性势能的计算
- 探究功与速度变化的关系的实验方法探究功与速度变化的关系的实验方法
- 动能的概念动能的概念
- 动能定理的内容和用法动能定理的内容和用法
- 动能定理解决多阶段运动问题动能定理解决多阶段运动问题
- 动能定理解决变力做功问题动能定理解决变力做功问题
- 动能定理解决水平变速圆周运动问题动能定理解决水平变速圆周运动问题
- 动能定理解决竖直面内变速圆周运动问题动能定理解决竖直面内变速圆周运动问题
- 动能定理解决抛体问题动能定理解决抛体问题
- 机械能守恒定律(III)机械能守恒定律(III)
- 机械能变化与力做功的关系机械能变化与力做功的关系
- 机械能守恒的条件和应用机械能守恒的条件和应用
- 机械能守恒时的能量转化机械能守恒时的能量转化
- 做功与能量变化关系的总结做功与能量变化关系的总结
- 天体的机械能天体的机械能
- 静摩擦力做功对系统机械能的影响静摩擦力做功对系统机械能的影响
- 滑动摩擦力做功对系统机械能的影响滑动摩擦力做功对系统机械能的影响
- 研究水平传送带对物体机械能的影响研究水平传送带对物体机械能的影响
- 研究倾斜传送带对物体机械能的影响研究倾斜传送带对物体机械能的影响
- 系统机械能守恒条件系统机械能守恒条件
- 系统机械能守恒的计算方法系统机械能守恒的计算方法
- 系统机械能守恒中的内力做功系统机械能守恒中的内力做功
- 验证机械能守恒的实验装置验证机械能守恒的实验装置
- 验证机械能守恒的数据处理验证机械能守恒的数据处理
- 能量守恒定律能量守恒定律
- 能量的耗散能量的耗散
- 水能的利用水能的利用
- 风能的利用风能的利用
- 太阳能的利用太阳能的利用
- 静电场(I)静电场(I)
- 电荷电荷
- 使物体带电的三种方式使物体带电的三种方式
- 电荷守恒定律 元电荷电荷守恒定律 元电荷
- 库仑定律库仑定律
- 库仑扭秤库仑扭秤
- 库仑定律的再讨论库仑定律的再讨论
- 两球接触后分开库仑力的计算两球接触后分开库仑力的计算
- 与静力学综合问题与静力学综合问题
- 电场强度的定义电场强度的定义
- 点电荷电场强度的叠加点电荷电场强度的叠加
- 带电体电场强度的叠加带电体电场强度的叠加
- 常见的电场分布常见的电场分布
- 匀强电场的产生和性质匀强电场的产生和性质
- 电场力作用下的平衡问题电场力作用下的平衡问题
- 电场力作用下的连接体问题电场力作用下的连接体问题
- 特殊带电体周围的场强分布特殊带电体周围的场强分布
- 静电场(II)静电场(II)
- 电势能电势能
- 电势电势
- 电势差电势差
- 等势面和等势线等势面和等势线
- 常见电场的电势分布常见电场的电势分布
- 电势的叠加问题电势的叠加问题
- 用等分法计算匀强电场中的电场与电势用等分法计算匀强电场中的电场与电势
- 实验:用描迹法绘制等势线实验:用描迹法绘制等势线
- 静电平衡静电平衡
- 导体上的电荷和电势分布导体上的电荷和电势分布
- 尖端放电尖端放电
- 静电屏蔽静电屏蔽
- 静电感应的多阶段变化问题静电感应的多阶段变化问题
- 范德格拉夫起电机的原理范德格拉夫起电机的原理
- 静电场(III)静电场(III)
- 电容器电容器
- 电容器的电容电容器的电容
- 电容器在Q不变时的探究电容器在Q不变时的探究
- 电容器在U不变时的探究电容器在U不变时的探究
- 电容器的能量和电量电容器的能量和电量
- 力的角度分析带电粒子的运动力的角度分析带电粒子的运动
- 密立根油滴实验密立根油滴实验
- 能量角度分析带电粒子的运动能量角度分析带电粒子的运动
- 电场中的动能定理和能量守恒电场中的动能定理和能量守恒
- 通过粒子轨迹研究粒子能量变化1通过粒子轨迹研究粒子能量变化1
- 通过粒子轨迹研究粒子能量变化2通过粒子轨迹研究粒子能量变化2
- 重力与电场力的共同作用问题重力与电场力的共同作用问题
- 重力与电场力共同作用下的计算重力与电场力共同作用下的计算
- 带电粒子在交变电压的电容器之间的运动带电粒子在交变电压的电容器之间的运动
- 带电粒子在交变电压的电容器之间的运动进阶带电粒子在交变电压的电容器之间的运动进阶
- 带电粒子在电容器中的偏转带电粒子在电容器中的偏转
- 带电粒子的屏幕落点带电粒子的屏幕落点
- 示波器原理示波器原理
- 示波器的面板示波器的面板
- 恒定电流(I)恒定电流(I)
- 电源电源
- 电流的定义式电流的定义式
- 电流的微观表达式电流的微观表达式
- 导体中的三个速度导体中的三个速度
- 电动势电动势
- 电动势与电势差电动势与电势差
- 电池的参数电池的参数
- 欧姆定律欧姆定律
- 伏安特性曲线伏安特性曲线
- 实验:描绘小灯泡的伏安特性曲线实验:描绘小灯泡的伏安特性曲线
- 串联电路的性质串联电路的性质
- 并联电路的性质并联电路的性质
- 复杂电路的识别与等效变换复杂电路的识别与等效变换
- 含表电路的化简含表电路的化简
- 电压表的改装电压表的改装
- 电流表的改装电流表的改装
- 非理想电表的计算非理想电表的计算
- 恒定电流(II)恒定电流(II)
- 电功率电功率
- 焦耳定律焦耳定律
- 焦耳定律的应用焦耳定律的应用
- 非纯电阻电路的能量关系非纯电阻电路的能量关系
- 伏安法测电阻的两种方式伏安法测电阻的两种方式
- 滑动变阻器的两种接法滑动变阻器的两种接法
- 限流法与分压法的再讨论限流法与分压法的再讨论
- 电阻率电阻率
- 金属电阻率的测量方法金属电阻率的测量方法
- 游标卡尺的结构和使用游标卡尺的结构和使用
- 螺旋测微器的结构和使用螺旋测微器的结构和使用
- 二极管的伏安特性二极管的伏安特性
- 恒定电流(III)恒定电流(III)
- 闭合电路欧姆定律闭合电路欧姆定律
- 闭合电路中的路端电压闭合电路中的路端电压
- 闭合电路中的功率和效率闭合电路中的功率和效率
- 闭合电路中的U-I图象问题闭合电路中的U-I图象问题
- 直流电路动态分析直流电路动态分析
- 含电容的直流电路分析含电容的直流电路分析
- 电源的串联和并联电源的串联和并联
- 测电源的电动势和内阻的实验方法测电源的电动势和内阻的实验方法
- 测电源的电动势和内阻的误差分析测电源的电动势和内阻的误差分析
- 测电源的电动势和内阻的其它方法测电源的电动势和内阻的其它方法
- 恒定电流(IV)恒定电流(IV)
- 欧姆表原理欧姆表原理
- 欧姆表的使用欧姆表的使用
- 多用电表多用电表
- 利用多用电表研究黑盒子问题利用多用电表研究黑盒子问题
- 电表校对电表校对
- 半偏法测电流表内阻半偏法测电流表内阻
- 半偏法测电压表内阻半偏法测电压表内阻
- 电桥法测电阻电桥法测电阻
- 其他测量电阻的方法其他测量电阻的方法
- 模拟电路和数字电路模拟电路和数字电路
- 逻辑与和与门逻辑与和与门
- 或门和非门或门和非门
- 门电路的物理实现门电路的物理实现
- 与非、或非、与或非门与非、或非、与或非门
- 同或门和异或门同或门和异或门
- 加法器加法器
- 逻辑电路与传感器逻辑电路与传感器
- 磁场(I)磁场(I)
- 磁现象和电流的磁效应磁现象和电流的磁效应
- 磁感应强度的定义磁感应强度的定义
- 磁感线磁感线
- 安培定则安培定则
- 安培分子电流假说安培分子电流假说
- 三种常见的电流磁场三种常见的电流磁场
- 磁场的叠加磁场的叠加
- 地磁场地磁场
- 电场与磁场的比较电场与磁场的比较
- 磁通量磁通量
- 磁通量的正负磁通量的正负
- 磁场(II)磁场(II)
- 安培力的方向安培力的方向
- 安培力的大小安培力的大小
- 电动机转动的原理电动机转动的原理
- 电流表的工作原理电流表的工作原理
- 通电直导线的相互作用通电直导线的相互作用
- 安培力作用下物体的运动安培力作用下物体的运动
- 通电导体棒的平衡问题通电导体棒的平衡问题
- 通电导体棒的运动问题通电导体棒的运动问题
- 安培力做功的特点和瞬时冲量安培力做功的特点和瞬时冲量
- 洛伦兹力的方向洛伦兹力的方向
- 洛伦兹力的大小洛伦兹力的大小
- 电视机显像管的工作原理电视机显像管的工作原理
- 电场力与洛伦兹力的比较电场力与洛伦兹力的比较
- 磁场(III)磁场(III)
- 带电粒子在匀强磁场中的几类运动带电粒子在匀强磁场中的几类运动
- 解决磁场中圆周运动的一般方法解决磁场中圆周运动的一般方法
- 带电粒子在圆弧有界磁场中的运动带电粒子在圆弧有界磁场中的运动
- 带电粒子在直线有界磁场中的运动带电粒子在直线有界磁场中的运动
- 在匀强电场和匀强磁场中偏转的区别在匀强电场和匀强磁场中偏转的区别
- 带电粒子在磁场中圆周运动的多解问题(1)带电粒子在磁场中圆周运动的多解问题(1)
- 带电粒子在磁场中圆周运动的多解问题(2)带电粒子在磁场中圆周运动的多解问题(2)
- 带电粒子在组合场中运动带电粒子在组合场中运动
- 带电粒子在复合场中运动的轨迹分析带电粒子在复合场中运动的轨迹分析
- 带电粒子在复合场中运动的能量分析带电粒子在复合场中运动的能量分析
- 带电物体在复合场中运动带电物体在复合场中运动
- 带电物体在复合场中运动的能量问题带电物体在复合场中运动的能量问题
- 速度选择器速度选择器
- 质谱仪质谱仪
- 回旋加速器回旋加速器
- 磁流体发电磁流体发电
- 电磁流量计电磁流量计
- 霍尔效应的原理霍尔效应的原理
- 霍尔效应的应用霍尔效应的应用
- 电磁感应(I)电磁感应(I)
- 划时代的发现划时代的发现
- 切割磁感线与感应电流的产生切割磁感线与感应电流的产生
- 磁通量变化与感应电流的产生磁通量变化与感应电流的产生
- 切割磁感线和磁通量变化切割磁感线和磁通量变化
- 感应电流方向的探究感应电流方向的探究
- 楞次定律的应用楞次定律的应用
- 磁场变化引起的感应电流方向判断磁场变化引起的感应电流方向判断
- 右手定则右手定则
- 右手定则与楞次定律的关系右手定则与楞次定律的关系
- 感应电流的安培力问题感应电流的安培力问题
- 楞次定律与能量守恒定律楞次定律与能量守恒定律
- 电磁感应(II)电磁感应(II)
- 法拉第电磁感应定律法拉第电磁感应定律
- 切割磁感线的电动势切割磁感线的电动势
- 有效切割长度有效切割长度
- 磁感应强度变化引起的感应电动势磁感应强度变化引起的感应电动势
- 两个公式的比较两个公式的比较
- 转动切割问题转动切割问题
- 法拉第圆盘法拉第圆盘
- 路端电压和电动势的区别路端电压和电动势的区别
- 动生电动势动生电动势
- 洛伦兹力能否做功洛伦兹力能否做功
- 感生电动势感生电动势
- 柱状磁场区域产生的涡旋电场柱状磁场区域产生的涡旋电场
- 电子感应加速器电子感应加速器
- 涡旋电场的场强大小涡旋电场的场强大小
- 电磁感应(III)电磁感应(III)
- 恒力作用下的单棒问题恒力作用下的单棒问题
- 电磁感应中安培力的功电磁感应中安培力的功
- 恒力作用下单棒的能量问题恒力作用下单棒的能量问题
- 电量计算电量计算
- 电量计算的复杂问题电量计算的复杂问题
- 磁通量正负变化与电量问题磁通量正负变化与电量问题
- 反电动势反电动势
- 金属棒在电源作用下的运动金属棒在电源作用下的运动
- 金属棒在不同形状轨道上的运动金属棒在不同形状轨道上的运动
- 不同形状的导体棒轨道上的运动的问题不同形状的导体棒轨道上的运动的问题
- 利用动量定理求电量利用动量定理求电量
- 金属框运动问题金属框运动问题
- 金属棒在变化的磁场中运动问题金属棒在变化的磁场中运动问题
- 电磁感应(IV)电磁感应(IV)
- 匀速运动下的含容问题匀速运动下的含容问题
- 变速运动下的含容问题变速运动下的含容问题
- 恒力作用下的含容问题恒力作用下的含容问题
- 电磁流量计电磁流量计
- 金属框在不同磁场中运动问题金属框在不同磁场中运动问题
- 磁悬浮列车磁悬浮列车
- 匀速运动的双棒问题匀速运动的双棒问题
- 只受安培力的双棒问题只受安培力的双棒问题
- 不等长的双棒问题不等长的双棒问题
- 恒力作用下的双棒问题恒力作用下的双棒问题
- 感应电动势、电流的图像问题感应电动势、电流的图像问题
- 其它类电磁感应图像问题其它类电磁感应图像问题
- 利用图像分析电磁感应问题利用图像分析电磁感应问题
- 电磁感应(V)电磁感应(V)
- 互感互感
- 自感自感
- 自感系数自感系数
- 小灯泡为何闪亮小灯泡为何闪亮
- 含电感的电路分析含电感的电路分析
- 自感的应用与防止自感的应用与防止
- 日光灯日光灯
- 涡流的热效应涡流的热效应
- 涡流的应用与防止涡流的应用与防止
- 电磁阻尼电磁阻尼
- 电磁驱动电磁驱动
- 交变电流(I)交变电流(I)
- 交流电和直流电交流电和直流电
- 正弦交流电的产生方式正弦交流电的产生方式
- 中性面和与中性面垂直的平面中性面和与中性面垂直的平面
- 任意时刻的感应电动势任意时刻的感应电动势
- 交流电的周期、频率和峰值交流电的周期、频率和峰值
- 交流电的平均值交流电的平均值
- 交流电有效值的含义交流电有效值的含义
- 正弦交流电的有效值正弦交流电的有效值
- 正弦交流电有效值的推导正弦交流电有效值的推导
- 交流发电机做电源时的电压、电流和电量交流发电机做电源时的电压、电流和电量
- 交流发电机做电源时的电功交流发电机做电源时的电功
- 交变电流(II)交变电流(II)
- 电感对直流电和交流电的不同作用电感对直流电和交流电的不同作用
- 电感对交流电的阻碍作用大小-感抗电感对交流电的阻碍作用大小-感抗
- 扼流圈扼流圈
- 电容对直流电和交流电的不同作用电容对直流电和交流电的不同作用
- 电容对交流电的阻碍大小-容抗电容对交流电的阻碍大小-容抗
- 电感和电容中储存的能量电感和电容中储存的能量
- 滤波器滤波器
- 变压器的结构变压器的结构
- 变压器的变压原理变压器的变压原理
- 变压器的功率和电流变压器的功率和电流
- 自耦变压器和多级输出变压器自耦变压器和多级输出变压器
- 互感器互感器
- 线圈存在电阻时的变压器线圈存在电阻时的变压器
- 输电模型中的电压问题输电模型中的电压问题
- 输电模型中的功率问题输电模型中的功率问题
- 更具体的远距离输电模型更具体的远距离输电模型
- 电网简介电网简介
- 传感器传感器
- 传感器是什么传感器是什么
- 位移和压力传感器位移和压力传感器
- 声音传感器和触摸屏声音传感器和触摸屏
- 电熨斗和电饭锅的温度传感器电熨斗和电饭锅的温度传感器
- 测温仪测温仪
- 光敏电阻光敏电阻
- 光传感器的应用光传感器的应用
- 干簧管干簧管
- 磁强计磁强计
- 分子动理论分子动理论
- 分子动理论的基本观点分子动理论的基本观点
- 油膜法测分子直径油膜法测分子直径
- 分子体积、摩尔体积、分子质量、摩尔质量的关系分子体积、摩尔体积、分子质量、摩尔质量的关系
- 扩散现象扩散现象
- 布朗运动布朗运动
- 分子热运动的统计规律分子热运动的统计规律
- 分子之间存在间隙分子之间存在间隙
- 分子之间的引力和斥力分子之间的引力和斥力
- 分子间作用力的进一步讨论1分子间作用力的进一步讨论1
- 分子间作用力的进一步讨论2分子间作用力的进一步讨论2
- 热平衡和温度热平衡和温度
- 温标温标
- 温度计温度计
- 分子动能分子动能
- 分子势能分子势能
- 分子势能的进一步讨论分子势能的进一步讨论
- 内能内能
- 气体气体
- 实验:研究气体的等温变化实验:研究气体的等温变化
- 玻意耳定律玻意耳定律
- 等温变化的P-V图像等温变化的P-V图像
- 查理定律查理定律
- 盖-吕萨克定律盖-吕萨克定律
- 理想气体理想气体
- 理想气体状态方程理想气体状态方程
- 随机性与统计规律随机性与统计规律
- 气体温度的微观意义气体温度的微观意义
- 气体压强的微观意义气体压强的微观意义
- 对气体实验定律的微观解释对气体实验定律的微观解释
- 固体、液体和物态变化固体、液体和物态变化
- 晶体和非晶体晶体和非晶体
- 晶体的微观结构晶体的微观结构
- 液体的微观结构液体的微观结构
- 表面张力表面张力
- 浸润和不浸润现象浸润和不浸润现象
- 毛细现象毛细现象
- 液晶液晶
- 蒸发蒸发
- 饱和汽与饱和汽压饱和汽与饱和汽压
- 湿度湿度
- 熔化热熔化热
- 汽化热汽化热
- 热力学定律热力学定律
- 焦耳实验焦耳实验
- 热量和热功当量热量和热功当量
- 热力学第一定律热力学第一定律
- 用热力学第一定律解释生活中的现象用热力学第一定律解释生活中的现象
- 能量守恒和永动机能量守恒和永动机
- 热力学第二定律的克劳修斯表述热力学第二定律的克劳修斯表述
- 热力学第二定律的开尔文表述热力学第二定律的开尔文表述
- 能量的品质能量的品质
- 开发新能源和可持续发展开发新能源和可持续发展
- 机械振动机械振动
- 什么是简谐运动什么是简谐运动
- 简谐运动的规律简谐运动的规律
- 简谐运动的图像简谐运动的图像
- 描述简谐运动的物理量描述简谐运动的物理量
- 简谐运动的回复力简谐运动的回复力
- 用参考圆分析简谐运动用参考圆分析简谐运动
- 简谐运动的表达式简谐运动的表达式
- 简谐运动的能量简谐运动的能量
- 简谐运动的对称性简谐运动的对称性
- 单摆单摆
- 单摆的周期单摆的周期
- 单摆的周期与摆长的关系单摆的周期与摆长的关系
- 单摆的周期与重力加速度的关系单摆的周期与重力加速度的关系
- 阻尼振动和无阻尼振动阻尼振动和无阻尼振动
- 受迫振动受迫振动
- 共振共振
- 机械波(I)机械波(I)
- 波的形成和传播条件波的形成和传播条件
- 横波和纵波横波和纵波
- 波的图像波的图像
- 在波的图像中判断质点运动方向在波的图像中判断质点运动方向
- 波长波长
- 频率和波速频率和波速
- 振动图像与波动图像振动图像与波动图像
- 波传播的综合性问题波传播的综合性问题
- 周期导致的多解性周期导致的多解性
- 波长导致的多解性波长导致的多解性
- 机械波(II)机械波(II)
- 惠更斯原理惠更斯原理
- 波的反射波的反射
- 波的折射波的折射
- 波的衍射波的衍射
- 衍射的定性分析衍射的定性分析
- 波的叠加原理波的叠加原理
- 叠加波型的判断叠加波型的判断
- 叠加波振动方向的判断叠加波振动方向的判断
- 波的干涉波的干涉
- 相干波源相干波源
- 加强点和减弱点的位置加强点和减弱点的位置
- 干涉的综合性问题干涉的综合性问题
- 声波的干涉声波的干涉
- 多普勒效应多普勒效应
- 多普勒效应频率变化计算多普勒效应频率变化计算
- 光(I)光(I)
- 光的折射光的折射
- 折射定律的应用折射定律的应用
- 折射定律的联系实际问题折射定律的联系实际问题
- 测定玻璃的折射率测定玻璃的折射率
- 测定玻璃折射率的误差分析测定玻璃折射率的误差分析
- 测定玻璃折射率的数据处理测定玻璃折射率的数据处理
- 相干光源相干光源
- 干涉条纹的加强与减弱干涉条纹的加强与减弱
- 干涉条纹的间距干涉条纹的间距
- 实验:测定光波的波长实验:测定光波的波长
- 测定光波波长的数据处理测定光波波长的数据处理
- 薄膜干涉薄膜干涉
- 检查平整度检查平整度
- 牛顿环牛顿环
- 增透膜增透膜
- 光的色散光的色散
- 虹和霓虹和霓
- 光(II)光(II)
- 光的衍射光的衍射
- 狭缝衍射狭缝衍射
- 其它衍射其它衍射
- 光的偏振光的偏振
- 偏振镜偏振镜
- 偏振的其他应用偏振的其他应用
- 全反射全反射
- 全反射棱镜全反射棱镜
- 光导纤维光导纤维
- 海市蜃楼海市蜃楼
- 平行玻璃砖平行玻璃砖
- 光在介质中传播的时间光在介质中传播的时间
- 全反射的临界态问题全反射的临界态问题
- 全反射与几何问题的综合计算全反射与几何问题的综合计算
- 激光的产生与特点激光的产生与特点
- 激光的应用激光的应用
- 电磁波电磁波
- 麦克斯韦电磁场理论麦克斯韦电磁场理论
- 振荡电路振荡电路
- 振荡电路的电压和电流关系振荡电路的电压和电流关系
- 电磁振荡的周期和频率电磁振荡的周期和频率
- 有效发射电磁波的条件有效发射电磁波的条件
- 电磁波的发射电磁波的发射
- 无线电波的接收无线电波的接收
- 电磁波的应用1电磁波的应用1
- 电磁波的应用2电磁波的应用2
- 电磁波谱的介绍电磁波谱的介绍
- 无线电波无线电波
- 红外线红外线
- 相对论简介相对论简介
- 伽利略相对性原理伽利略相对性原理
- 迈克尔孙-莫雷实验和光速不变原理迈克尔孙-莫雷实验和光速不变原理
- 相对性原理和协变性相对性原理和协变性
- 同时的相对性同时的相对性
- 长度的相对性长度的相对性
- 长度收缩的再讨论长度收缩的再讨论
- 时间间隔的相对性时间间隔的相对性
- 狭义相对论的实验验证狭义相对论的实验验证
- 相对论质量相对论质量
- 相对论动量和能量相对论动量和能量
- 广义相对论的基本原理广义相对论的基本原理
- 惯性力惯性力
- 广义相对论的几个结论广义相对论的几个结论
- 动量守恒定律(I)动量守恒定律(I)
- 动量动量
- 冲量冲量
- 动量定理的推导和内容动量定理的推导和内容
- 利用动量定理求平均冲力利用动量定理求平均冲力
- 动量定理与动能定理的比较动量定理与动能定理的比较
- 利用动量定理求力的冲量或动量变化量利用动量定理求力的冲量或动量变化量
- 利用动量定理求解多过程问题利用动量定理求解多过程问题
- 利用动量定理解决流体冲击力问题利用动量定理解决流体冲击力问题
- 动量定理应用于质点组问题动量定理应用于质点组问题
- 动量守恒定律的内容和条件动量守恒定律的内容和条件
- 动量守恒定律的计算动量守恒定律的计算
- 分方向上的动量守恒定律分方向上的动量守恒定律
- 动量守恒定律解决多物多过程问题动量守恒定律解决多物多过程问题
- 动量守恒定律解决递推问题动量守恒定律解决递推问题
- 用动量守恒定律解决临界问题用动量守恒定律解决临界问题
- 动量守恒定律(II)动量守恒定律(II)
- 碰撞的分类碰撞的分类
- 弹性碰撞弹性碰撞
- 速度互换的应用速度互换的应用
- 完全非弹性碰撞完全非弹性碰撞
- 碰撞需满足的条件碰撞需满足的条件
- 其他类碰撞问题其他类碰撞问题
- 反冲运动反冲运动
- 人船问题人船问题
- 火箭火箭
- 动量机械能综合问题(一)动量机械能综合问题(一)
- 动量机械能综合问题(二)动量机械能综合问题(二)
- 波粒二象性波粒二象性
- 黑体黑体
- 黑体辐射黑体辐射
- 能量子能量子
- 光电效应光电效应
- 光电效应的产生条件光电效应的产生条件
- 最大初动能最大初动能
- 饱和光电流饱和光电流
- 光子光子
- 光电效应方程光电效应方程
- 光电效应的综合性问题光电效应的综合性问题
- 密立根实验密立根实验
- 康普顿散射康普顿散射
- 光子的动量光子的动量
- 光的波粒二象性光的波粒二象性
- 粒子的波动性粒子的波动性
- 概率波概率波
- 不确定关系不确定关系
- 原子结构原子结构
- 电子的发现电子的发现
- 电子的电量和质量的测定电子的电量和质量的测定
- 汤姆孙模型汤姆孙模型
- α粒子散射实验α粒子散射实验
- 原子核式结构模型原子核式结构模型
- 原子的尺度原子的尺度
- 光谱的分类光谱的分类
- 氢原子光谱的实验规律氢原子光谱的实验规律
- 经典理论的困难经典理论的困难
- 玻尔的假设玻尔的假设
- 玻尔理论对氢光谱的解释玻尔理论对氢光谱的解释
- 玻尔模型的局限性玻尔模型的局限性
- 能级跃迁与电离能级跃迁与电离
- 原子激发的两种方式与能量变化原子激发的两种方式与能量变化
- 弗兰克赫兹实验弗兰克赫兹实验
- 原子核(I)原子核(I)
- 天然放射性现象天然放射性现象
- 三种射线三种射线
- 原子核的组成原子核的组成
- 放射性元素的衰变放射性元素的衰变
- 衰变中的动量守恒衰变中的动量守恒
- 半衰期半衰期
- 对半衰期的再讨论对半衰期的再讨论
- 探测射线的方法探测射线的方法
- 人工核反应和放射性同位素人工核反应和放射性同位素
- 放射性的应用和防护放射性的应用和防护
- 原子核(II)原子核(II)
- 原子核中质子与中子的比例原子核中质子与中子的比例
- 结合能结合能
- 质量亏损质量亏损
- 核裂变核裂变
- 链式反应链式反应
- 核反应堆核反应堆
- 核聚变核聚变
- 基本粒子基本粒子
- 夸克模型夸克模型
- 天体与宇宙天体与宇宙
《理想气体状态方程》理想气体状态方程
1多选题
(多选)如图为竖直放置的上细下粗的密闭细管,水银柱将气体分隔成A、B两部分,初始温度相同.使A、B升高相同温度达到稳定后,体积变化量为△V_A、△V_B,压强变化量为△p_A、△p_B,对液面压力的变化量为△F_A、△F_B,则( )
题目答案
您的答案
答案解析
分析:
本题可采取假设法,假设气体的体积不变,根据等容变化判断出上下气体的压强变化量以及压力变化量,从而判断出水银柱的移动方向.关于体积的变化量关系,可抓住总体积不变去分析.
解答:
解:首先假设液柱不动,则A、B两部分气体发生等容变化,由查理定律,对气体A:$\frac {P_A}{T_A}$=$\frac {P_A}{T_A}$;对气体B:$\frac {P_B}{T_A}$=$\frac {P_B}{T_A}$,又初始状态满足P_A=P_B+h,可见使A、B升高相同温度,P_A_=$\frac {T_A}{T_A}$P_A=$\frac {T_A}{T_A}$(P_B+h),P_B_=$\frac {T_A}{T_A}$P_B,因此△P_A>△P_B,因此△F_A>△F_B液柱将向上移动,A正确,C正确;由于气体的总体积不变,因此△V_A=△V_B,所以B、D错误.
故选AC.
点评:
解决本题的关键是选择合适的方法,假设法在本题中得到了很好的应用.
2单选题
下列说法中正确的是( )
题目答案
您的答案
答案解析
分析:
根据气体状态方程$\frac {PV}{T}$=C和已知的变化量去判断其它的物理量.
知道气体压强产生的原理.
解答:
解:A、一定质量的气体被压缩时,体积V减小,
根据气体状态方程$\frac {PV}{T}$=C,由于不清楚温度的变化,所以气体压强不一定增大.故A正确.
B、一定质量的气体温度不变压强增大时,根据气体状态方程$\frac {PV}{T}$=C,其体积应减小.故B错误.
C、气体分子相距较远,相互间的作用力很小,有较好的流动性,由于大量分子都在不停地做无规则热运动,与器壁频繁碰撞,使器壁受到一个平均持续的冲力,致使气体对器壁产生一定的压强.故C错误.
D、气体的压强是气体分子与器壁碰撞产生与是否处于失重状态无关,故D错误.
故选A.
点评:
能够运用控制变量法研究多个物理量变化时的关系.
我们要了解固体和液体压强与气体压强的产生原理.
3多选题
(多选)如图所示,U形管A、B内装有一部分水银,通过橡胶软管与玻璃管C相连,C管竖直插入水银槽中,若A、B、C三管内径相同,U形管两侧液面高度差为h,中间封有一段空气,则( )
题目答案
您的答案
答案解析
分析:
根据AB水银面的高度差求出封闭气体的压强,再确定C管内外水银面的高度差.若将C管向下移动少许,封闭气体的压强增大,B管内水银面沿管壁上升.若往B管注入一些水银,封闭气体的压强增大,气体的体积减小,A管水银面上升的高度大于C管水银面下降的高度.若环境温度升高,封闭气体的压强增大,A管水银面下降的高度大于C管水银面下降的高度.
解答:
解:
A、设C管内外水银面的高度差为h′,则封闭气体的压强为
P_0+h=P_0+h′,则有h′=h,即C管内外水银面的高度差为h.故A正确.
B、若将C管向下移动少许,封闭气体的压强增大,B管内水银面沿管壁上升.故B正确.
C、若往B管注入一些水银,封闭气体的压强增大,根据玻意耳定律可知,气体的体积减小,A管水银面上升的高度大于C管水银面下降的高度.故C正确.
D、若环境温度升高,封闭气体的压强增大,A管水银面下降的高度大于C管水银面下降的高度.故D错误.
故选ABC
点评:
本题关键是确定封闭气体压强如何变化,也可以采用假设法理解.基础题.
4多选题
(多选)如图所示,一根竖直的弹簧支持着一倒立气缸的活塞,使气缸悬空而静止,设活塞与缸壁间无摩擦且可以在缸内自由移动,缸壁导热性能良好使缸内气体总能与外界大气温度相同,则下述结论中正确的是( )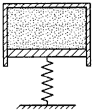
题目答案
您的答案
答案解析
分析:
理想气体的等温变化PV=C(常数),等压变化$\frac {V$_1$}{T$_1$}$=C,然后结合选项合理选择整体法与隔离法.
解答:
解:A、选择气缸和活塞为整体,那么整体所受的大气压力相互抵消,若外界大气压增大,则弹簧长度不发生变化,故A错误.
B、选择气缸内为研究对象,竖直向下受重力和大气压力PS,向上受到缸内气体向上的压力P$_1$S,物体受三力平衡:G+PS=P$_1$S,若外界大气压P增大,P$_1$一定增大,根据理想气体的等温变化PV=C(常数),当压强增大时,体积一定减小,所以气缸的上底面距地面的高度将减小,故B正确.
C、选择气缸和活塞为整体,那么整体所受的大气压力相互抵消,当气温升高时,则弹簧长度不发生变化,则活塞距地面的高度不变,故C错误.
D、若气温升高,缸内气体做等压变化,根据:$\frac {V$_1$}{T$_1$}$=C,当温度升高时,气体体积增大,气缸上升,则气缸的上底面距地面的高度将增大,故D正确.
故选BD.
点评:
在理想气体状态方程的应用中,关键判断P、V、T三个物理量中哪个是不变量.
5多选题
(多选)一定质量的某理想气体,处在某一状态,经下列哪个过程后回到原来的温度( )
题目答案
您的答案
答案解析
分析:
根据题意,应用力学气体状态方程分析答题.
解答:
解:A、由理想气体状态方程:$\frac {pV}{T}$=C可知,保持压强不变而使它的体积膨胀,温度T升高,接着保持体积不变而减小压强,温度降低,温度可能回到原来的温度,故A正确;
B、由理想气体状态方程:$\frac {pV}{T}$=C,先保持压强不变而使它的体积减小,温度降低,接着保持体积不变而减小压强,温度继续降低,温度不可能回到原来的温度,故B错误;
C、由理想气体状态方程:$\frac {pV}{T}$=C,先保持体积不变而增大压强,温度升高,接着保持压强不变而使它的体积膨胀,温度继续升高,温度不可能回到原来的值,故C错误;
D、由理想气体状态方程:$\frac {pV}{T}$=C,先保持体积不变而减小压强,温度降低,接着保持压强不变而使它的体积膨胀,温度升高,温度可能回到原来的温度,故D正确;
故选:AD.
点评:
本题考查了判断气体温度变化情况,应用理想气体状态方程即可正确解题.
6单选题
关于理想气体的状态变化,下列说法中正确的是( )
题目答案
您的答案
答案解析
分析:
对于一定质量的理想气体$\frac {pV}{T}$=C,各个选项逐一分析.
解答:
解:A、一定质量的理想气体,压强不变时,体积与热力学温度成正比,温度由100K上升到200K时,体积增大到原来的2倍,故A错误;
B、气体由状态1到状态2,一定满足方程$\frac {p$_1$V$_1$}{T$_1$}$=$\frac {p$_2$V$_2$}{T$_2$}$,必须满足质量不变,故B错误;
C、根据气体状态方程$\frac {pV}{T}$=C,一定质量的理想气体体积增大到原来的4倍,可能是压强减半,热力学温度加倍,故C正确;
D、根据理想气体状态方程$\frac {pV}{T}$=C,“压强增大到原来的4倍,可能是体积加倍,热力学温度减半”则比值增大,故D错误;
故选:C
点评:
本题考查了气体状态参量如果变化,根据题意求出气体状态参量应用理想气体状态方程可以解题,解题时注意假设法的应用.